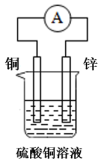
 B .
B . 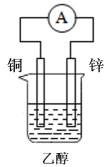 C .
C . 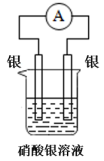 D .
D . 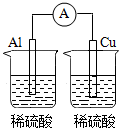
|
|
|
|
A.西汉彩绘陶钟的主要成分是碳酸钙( | B.泥土属于混合物 | C.酸雨对莲花纹石柱有严重的破坏作用 | D.常温下铁在浓硫酸中会钝化 |
选项 | 实验目的 | 实验过程 |
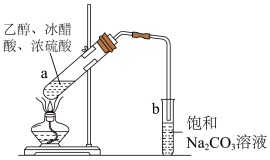
A | 探究浓硫酸的脱水性和强氧化性 | 把浓硫酸滴入蔗糖中,并将产生的气体通入澄清石灰水中,观察实验现象 |
B | 探究反应物浓度对反应速率的影响 | 向分别盛有 |
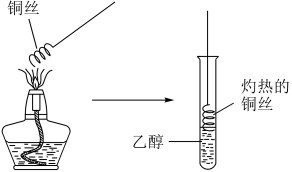
C | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,观察是否有无色气体产生 |
D | 确认二氯甲烷分子不存在同分异构体 | 先搭建甲烷分子球棍模型,后用2个氯原子取代任意2个氢原子,重复数次,观察所得球棍模型的结构 |
![]() 、
、![]() 、分别表示
、分别表示、催化剂)
![]()
时间 | | | | |
0 | 0.40 | 1.00 | 0 | 0 |
5 | | 0.80 | | 0.60 |
7 | 0.20 | 0.80 | 0.20 | 0.60 |
分析表中数据,判断时反应是否处于平衡状态?(填“是”或“否”)。
内,用
的浓度变化表示的平均反应速率为
。

装置A中生石灰的作用是实验室也常用氯化铵和氢氧化钙混合固体制取氨气,写出发生反应的化学方程式。
a.甲、乙都是碱石灰 b.甲、乙都是无水氯化钙
c.甲是碱石灰,乙是五氧化二磷 d.甲是浓硫酸,乙是碱石灰
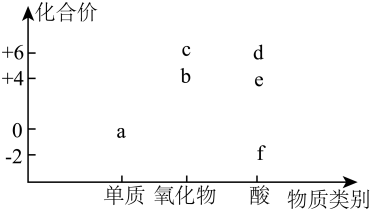
Ⅰ.如图是元素周期表的一部分,回答下列问题:

资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
序号 | 实验① | 实验② |
实验操作 |
|
|
现象 | 溶液变为黄色 |
实验①可得出氧化性强弱:。
实验③ | 另取实验①反应后的黄色溶液少许,先加入足量的 |
补做实验③的目的是。
加入的试剂1、2分别是、。

①写出“氧化”过程中发生反应的离子方程式。
②将吹出后的含空气按一定速率通入吸收塔,用
和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式;吹出时
的吹出率与吸收塔中
流量的关系如图所示。
流量过大,
吹出率反而下降的原因是。
