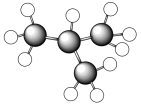
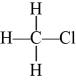 与
与 D .
D . 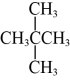
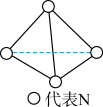
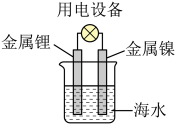
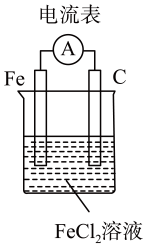 B .
B . 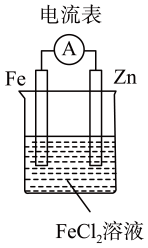 C .
C . 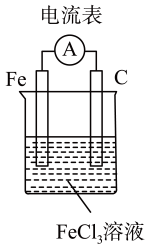 D .
D . 
选项 | 实验操作 | 实验目的 |
A | 取少量样品于试管中,加入稀 | 判断样品中是否含有 |
B | 将炽热的木炭与浓硫酸混合后所得气体通入澄清石灰水中 | 验证碳的氧化产物为 |
C | 将适量 | 比较Cl和Si元素非金属强弱 |
D | 其他条件相同, | 探究温度对反应速率的影响 |
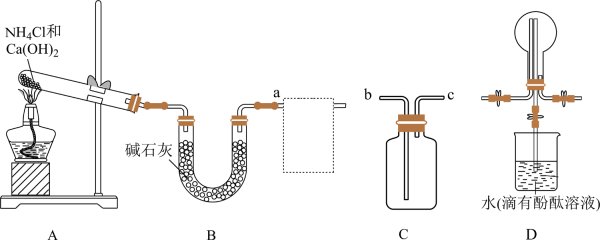
①A中制取氨气的化学方程式为。
②C为方框内氨气的收集装置,则a应与(填“b”或“c”)相连。
③证明氨气已集满的操作和现象是。
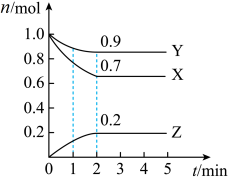
a.X、Y、Z三种气体的浓度相等
b.混合气体的相对分子质量不随时间变化
c.混合气体的总压强不随时间变化
d.反应速率
e.
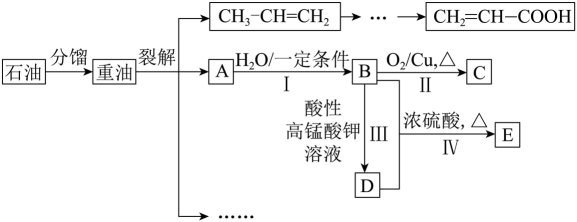
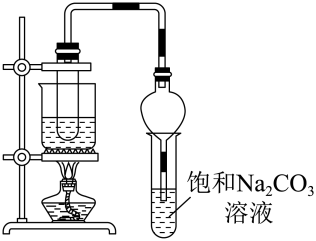
①反应Ⅳ的化学方程式为。
②球形漏斗的主要作用是。
③若实验所用D质量为6.0 g,B质量为5.0 g,得到纯净产品E质量为6.6 g,则E的产率是多少(写出计算过程)?