选项 | 劳动项目 | 化学知识 |
A | 煮水时,若水的硬度大,易结垢 | 硬水中含有较多可溶性钙、镁化合物 |
B | 用明矾处理较浑浊的天然水 | 明矾主要起杀菌消毒作用 |
C | 在盐田中晾晒海水,得到粗盐 | 粗盐除去泥沙即可得到纯净的氯化钠 |
D | 用洗涤剂清洗污渍 | 洗涤剂可以溶解油污 |
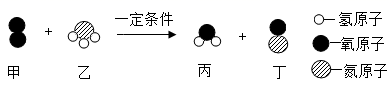
选项 | 混合物(括号内为杂质) | 试剂及方法 |
A | KCl溶液(K2CO3) | 滴加过量稀硫酸 |
B | HCl溶液(H2SO4) | 滴加适量氯化钡溶液,过滤 |
C | FeCl2溶液(CuCl2) | 加过量锌粉,过滤 |
D | N2(O2) | 通过灼热的氧化铜 |
 加热高锰酸钾制取氧气
B .
加热高锰酸钾制取氧气
B . 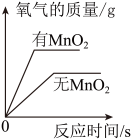 分解等质量等浓度的过氧化氢溶液
C .
分解等质量等浓度的过氧化氢溶液
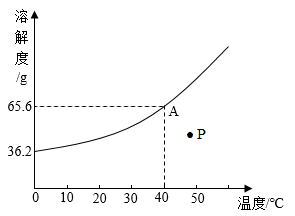
C .  将等质量的镁片、铁片加入足量稀硫酸中
D .
将等质量的镁片、铁片加入足量稀硫酸中
D .  用燃烧红磷的方法测定空气中氧气含量
用燃烧红磷的方法测定空气中氧气含量
A.84消毒剂(主要成分是NaClO) B.过氧化氢 C.氯气 D.过氧乙酸(C2H4O3)
①酸雨是导致土壤呈酸性的原因之一,酸雨的pH<。
②下列空气污染物会导致酸雨的是(多选,填字母序号)。
a.CO2 b.SO2 c.NO2 d.CO
Ⅰ.根据下列装置图,回答有关问题:
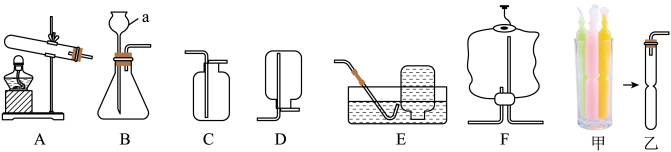
实验步骤:①计算,需要氯化钠的质量为g,②称量,③量取,④溶解,⑤转移,⑥贴标签备用。
实验步骤 | 实验现象 | 实验结论 |
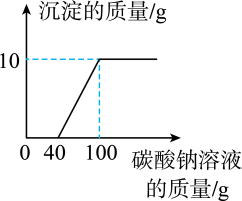
分别用a,b,c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 b中无明显现象 c中 | a中物质是稀盐酸 b中物质是食盐水 c中物质是澄清石灰水 |
写出a试管中发生反应的化学方程式:。
把c试管反应后的物质进行过滤,得到滤液。
【提出问题】滤液中溶质的成分是什么?
猜想一:Na2CO3和NaOH;
猜想二:NaOH;
猜想三:。
【实验过程】为证明猜想一是否正确,进行了如下实验
实验步骤 | 实验现象 | 实验结论 |
取一定量滤液于试管中,加入一种盐溶液(写化学式) | 有白色沉淀 | 猜想一正确 |
写出上述有白色沉淀生成的化学方程式:。
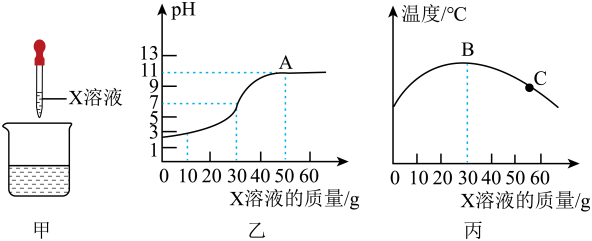
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值。
用pH试纸测定a试管反应后废液酸碱性的过程 | 测定结果 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取。(写操作过程) | pH<7(废液显酸性) |
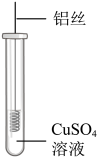
铝丝表面未出现红色物质,原因是。
填写实验报告单:
序号 | 实验现象 | 结论与解释 |
① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是;蓝绿色物质成分待探究 |
② | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是,说明Al能和CuSO4溶液反应,但反应较慢 |
③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度(填“>”或“<”)CuSO4溶液的密度 |
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为。
铝制品有较好的抗腐蚀性,其原因是。(用化学方程式表示)