 B . 用托盘天平称量氢氧化钠
B . 用托盘天平称量氢氧化钠 C . 用酚酞试液鉴别碳酸钠溶液和石灰水
C . 用酚酞试液鉴别碳酸钠溶液和石灰水 D . 稀释浓硫酸
D . 稀释浓硫酸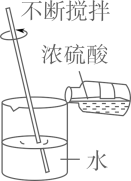

①苛性钠 ②碳酸钠晶体 ③浓盐酸 ④浓硫酸 ⑤生石灰
![]()
| pH | <6.5 | 7.0—7.1 | 7.5—8.5 | 8.5—12.0 | >12.5 |
| 颜色 | 粉红色 | 紫色 | 蓝色 | 绿色 | 黄色 |
3NaOH+AlCl3=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,NaAlO2易溶于水。下列图像正确的是( )
 B .
B .  C .
C .  D .
D . 

选项 | 物质 | 杂质 | 除杂所用的试剂和方法 |
A | ACaCl固体 | CaCO3固体 | 加入适量的稀盐酸 |
B | BNaOH溶液 | Ca(OH)2溶液 | 先加入适量的Na2CO3溶液,再过滤 |
C | CO2气体 | CO气体 | 点燃 |
D | DH2气体 | HCl气体 | 通过NaOH溶液洗气 |


| 烧杯中的物质 | x溶液 | | |
| A | 稀盐酸和硫酸铜溶液 | 烧碱溶液 | |
| B | 稀硫酸和稀盐酸 | 氯化钡溶液 | |
| C | 镁铝合金 | 稀盐酸 | |
| D | 氯化钠和碳酸氢钠溶液 | 稀盐酸 |






【提出问题】
氯化氢(HCl)气体显酸性吗?
【进行实验】
该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,取三朵用紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图所示的三个实验:

【实验现象】
Ⅰ和Ⅱ中小花不变色,Ⅲ中小花变红色。
【查阅资料】
氯化氢气体溶于水后能电离出H+和Cl-。
【实验结论】
【交流反思】
⑴从微观角度分析氯化氢气体不显酸性的原因是。
⑵紫甘蓝的汁液在酸性溶液中显色。
第一步,查阅资料,获取信息。
①氧化镁为白色固体
②镁与氮气化合能生成氮化镁(Mg3N2)
③氮化镁可与水剧烈反应产生氨气,该气体能溶于水形成碱性溶液。
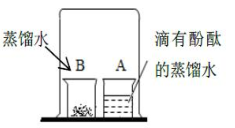
第二步,实验探究。取燃烧产物放入如图的烧杯B中,加入适量蒸馏水,用大烧杯罩住小烧杯A和B,观察到现象,从而确定黄色固体是Mg3N2。请写出判断的思路;写出镁与氮气反应生成氮化镁的化学方程式。

实验原理:测定下图C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
查阅资料:①CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生;
②饱和碳酸氢钠可以吸收HCl气体,且发生反应的化学方程式为;
③CO2不会溶于饱和碳酸氢钠溶液。实验装置如下图

根据探究过程回答下列问题:


①加BaCl2是为了除去;
②不能用 KOH 溶液代替NaOH,其原因是;
③通过操作Ⅲ所得滤液中的溶质有(用化学式表示);
④操作Ⅳ中加入一定量的盐酸调pH=7的目的是。
试验编号 | 一 | 二 | 三 |
试管内试剂 | Fe2O3粉末 | NaOH溶液+酚酞试剂 | MgCl2溶液 |
已知:对Cl﹣的检验、测定有干扰。

①沉淀A的化学式。
②步骤II中加入的试剂要足量,目的是。
③若满足m=(用含m1和m2的式子表示),证明实验三未发生复分解反应

测量次数 | 第1次 | 第6次 | 第16次 | 第21次 | 第26次 |
滴加的稀盐酸总质量/g | 0 | 5 | 15 | 20 | 25 |
溶液总质量/g | 50 | 55 | m | 69.78 | 74.78 |
溶液pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |

请分析计算: