 B . 过滤
B . 过滤  C . 称量固体
C . 称量固体  D . 收集氧气
D . 收集氧气 
选项 | 宏观现象 | 微观解释 |
A | 水沸腾时能掀开壶盖 | 分子的大小随温度的升高而增大 |
B | 湿衣服在太阳晒着的地方干得快 | 说明分子的运动速率与温度有关 |
C | 6000mL氮气可以压缩在40mL钢瓶中 | 增大压强可以减小分子间间隔 |
D | 电解水生成氢气和氧气 | 分子在化学变化中可以再分 |
选项 | 特鉴别的物质 | 鉴别方法 |
A | 二氧化碳和氮气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
B | 硬水和软水 | 分别加等量肥皂水,振荡,观察产生泡沫情况 |
C | 过氧化氢溶液和水 | 分别加入等量二氧化锰粉末,观察有无气泡产生 |
D | 氧气和空气 | 分别伸入带火星的木条,观察木条是否复燃 |
①两个氮分子:2N2:
②由三个氧原子构成的臭氧分子:30:
③粒子结构示意图 表示的粒子:S:
表示的粒子:S:
④两个铁离子:2Fe3+;
⑤相对分子质量最小的氧化物:H2O:
⑥+2价的镁元素:Mg2+。其中正确的有( )
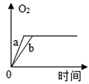 B .
B . 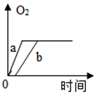 C .
C . 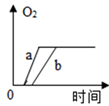 D .
D . 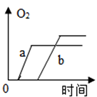
 B . 测空气中氧气的含量
B . 测空气中氧气的含量 C . 监控氧气的流速
C . 监控氧气的流速 D . 验证分子在不断运动
D . 验证分子在不断运动
同学们,你们知道潜水用的钢瓶中装的是什么气体吗?其实,这种气体既不是氧气,也不是普通的空气,
而是一种特殊的空气--人造空气。人造空气是将普通空气中的氮气除去后,把氧气和氦气按照1:4的比例
混合起来制成。这种人造空气中的氦气,极难溶于水,可以防止潜水员从深海处上升体内恢复常压时产生
氮气泡造成的“气塞症”。人造空气的密度只有普通空气的1/3,呼吸起来也比普通空气轻松得多,可以减
轻人呼吸的困难,因此还常用于治疗支气管哮喘等疾病。


。若用装置E收集氧气,验满的方法。

铝的化学式为。
【探究一】影响过氧化氢分解快慢的因素某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。
(实验装置如图1所示,夹持仪器已略去)

【猜想与假设】影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂种类。
【实验记录】同学们进行6组实验,实验记录如下:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | ---- | ---- | ---- | ---- | 0.5 gNaCl | 0.5 gFeCl3 |
60min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
【解释与结论】
同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是。
【探究二】:硫酸铜溶液也能做过氧化氢分解反应的催化剂,小组同学在常温下,向a,b,c三个试管中分别加入等量的5%的过氧化氢溶液,在其他条件相同时,各滴入2滴5%、10%、20%的硫酸铜溶液,绘制了产生氧气的体积和时间变化的曲线如图。请你回答:

写出两条规律性结论: