选项 | A | B | C | D |
工艺品 |
|
|
|
|
名称 | 光彩烧瓷 | 广州玉雕 | 佛山丝绸“香云纱” | 潮汕铜镜 |
选项 | 劳动项目 | 化学知识 |
A | 研究性学习活动:焊接两根铁棒 | 铝粉与氧化铁发生的铝热反应 |
B | 学农活动:用 NH4HCO3肥料施肥 | NH4HCO3受热易分解 |
C | 军训实践课:用镁条制造信号弹和焰火 | 镁条燃烧时发出耀眼白光 |
D | 艺术品制作:制作各种形状的石膏模型 | 熟石膏与水混合成糊状后能很快凝固 |


选项 | 实验方案 | 实验目的 |
A | 将SO2和CO2分别通入水中达到饱和,用pH计立即测定溶液的pH,比较pH大小 | 确定亚硫酸和碳酸的酸性强弱 |
B | 向反应后试管中加入水观察溶液变蓝色 | 验证Cu和浓硫酸反应生成CuSO4 |
C | 将SO2通入NaHCO3溶液后,将混合气体依次通入酸性KMnO4溶液、品红溶液、澄清石灰水 | 验证非金属性:S>C |
D | 向盛有1mL0.1mol•L-1NaCl溶液的试管中滴加5滴0.1mol•L-1AgNO3溶液,有白色沉淀生成,向其中继续滴加5滴0.1mol•L-1KI溶液,有黄色沉淀产生 | 验证:Ksp(AgI)<Ksp(AgCl) |



I.制取氯酸钾
利用如下左图所示的实验装置进行实验。回答下列问题:


试管编号 | 1 | 2 | 3 | 4 |
0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 5.0 | 0 |
取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
①3号试管实验中x的值为;1号试管实验的作用是。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为。
③由该系列实验可得出的结论是。

已知:为强电解质;P2O4为磷酸二异辛酯。
回答下列问题:
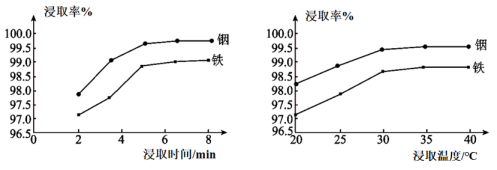
反应I: R(aq)+Cl-(aq) ⇌RCl-(aq)
反应II:RCl-(aq)+Cl-(aq) ⇌RCl(aq)
回答下列问题:
R+CH3CH2OHH2O +。
①0~15s内,Cl-的平均消耗速率v(Cl-)=。
②待反应充分进行,达到平衡状态时溶液的体积为V0 , 加蒸馏水稀释至溶液体积为V,达到新平衡时,Cl-的物质的量浓度为c平(Cl-),RCl的物质的量浓度为c平(RCl
)。写出反应I平衡常数的表达式KI=,稀释过程中平衡常数KI的值(填“变大”、“变小”或“不变”),请在答题卡坐标内画出
![]() 随1g
随1g的变化趋势曲线。
0 | 0.25 | 0.50 | 0.75 | 1.00 | ||
Cl- | 1.00 | 0.79 | 0.64 | 0.54 | 0.46 | |
RCl- | 0 | 0.09 | 0.16 | 0.22 | 0.28 | |
RCl22- | 0 | 0.06 | b | d | 0.13 | |
①从表格中数据可看出关系式:+
+2×
=1,则d=;此关系式也可从理论上推导,下列理论依据中,可推导该关系式的有(填选项序号)。
A.能量守恒定律 B.电荷守恒定律 C.质量守恒定律
D.氧化还原反应遵循还原剂失去的电子总数和氧化剂得到的电子总数相等的规律
②=0.50时,R的转化率为。
Ⅰ.苯环上只有三个取代基
Ⅱ.核磁共振氢谱图中只有4组吸收峰
Ⅲ.1mol该物质与足量NaHCO3溶液反应生成2mol CO2
 为原料制备
为原料制备 的合成路线流程补充完整(填写括号内的试剂与产物,无机试剂任选)。
的合成路线流程补充完整(填写括号内的试剂与产物,无机试剂任选)。