 B . 点燃酒精灯
B . 点燃酒精灯 C . 加热液体
C . 加热液体 D . 读取液体体积
D . 读取液体体积
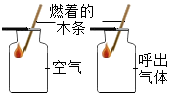 B . 验证氢气密度小于空气
B . 验证氢气密度小于空气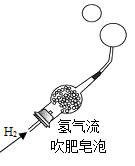 C . 证明蜡烛中含有碳元素
C . 证明蜡烛中含有碳元素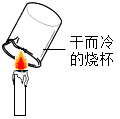 D . 探究分子运动
D . 探究分子运动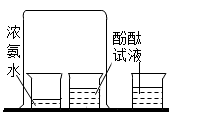
| 物质 | M | N | P | Q |
| 反应前物质的量/g | 18 | 1 | 2 | 32 |
| 反应后物质的量/g | 待测 | 26 | 2 | 12 |
①化学变化往往伴随着能量的变化,有能量变化的一定属于化学变化
②氧化物都含有氧元素,所以含氧元素的化合物不一定是氧化物
③同种元素的粒子质子数一定相同,质子数相同的粒子一定属于同种元素
④燃烧一般都伴随发光、发热现象,所以有发光、发热现象的变化就是燃烧
⑤单质是由同种元素组成的,则由同种元素组成的物质一定是单质
⑥原子、分子不带电,但不带电的微观粒子不一定都是分子和原子
| A向一定量锌粉中滴加稀盐酸 | B向一定量碳酸钙中加入稀盐酸 | C.加热一定量高锰酸钾固体,锰元素的质量分数变化 | D.向盛有二氧化锰的烧杯中加过氧化氢溶液 |
 |  |  |  |
①氧气 ②氮气 ③氢气 ④酒精 ⑤石墨 ⑥一氧化碳


a.金刚石、石墨、C60物理性质不同的原因;
b.一氧化碳、二氧化碳化学性质不同的原因。
取四朵用石蕊溶液染成紫色的干燥纸花,完成图示实验并回答下列问题。

对比实验Ⅰ和Ⅱ,说明水不能使石蕊变红,而 ;实验Ⅲ中紫色小花(填“变红色”或“不变色”);完成实验后,得到的结论是;实验Ⅳ结束后,将Ⅳ中的小花取出烘干,发生反应的化学方程式为 。



①原子数目②分子数目③元素种类④物质种类⑤原子种类⑥物质的总质量


①目前世界上多数国家利用的能量主要来自煤、石油和等化石燃料的燃烧。在工业上,利用石油中各成分的不同将它们分离,得到汽油、柴油等产品。
②为了节省石油资源,在一定程度上减少汽车尾气的污染,推广使用乙醇汽油,乙醇属于(填“可再生”或“不可再生”)能源。

①对比图1中铜片上的白磷和红磷的现象,说明燃烧的条件之一是;对比图1中铜片上的白磷和图3白磷的现象,说明燃烧的条件之一是;
②图2和图1相比,图2的优点是。(NaOH溶液可吸收燃烧生成物)

| 实验 | 1 | 2 | 3 | 4 |
| 加入盐酸的质量(g) | 50 | 50 | 50 | 50 |
| 生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |