

①用氢氧化钠溶液洗涤石油中残余的硫酸②用含氢氧化铝的药物治疗胃酸过多
③用熟石灰改良酸性土壤
④将稀氨水(含有、OH-)涂抹在蚊虫叮咬处(分泌出蚁酸)能止痒
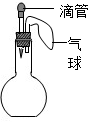
选项 | 滴管内物质 | 平底烧瓶内物质 |
A | 稀盐酸 | 锌粒 |
B | 氢氧化钙溶液 | 二氧化碳气体 |
C | 浓硫酸 | 水 |
D | 碳酸钠溶液 | 稀硫酸 |
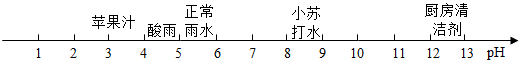

①t1℃时,甲、乙饱和溶液中溶质的质量相等
②甲、乙、丙三种固体物质的溶解度大小关系是:甲>乙>丙
③t2℃时,乙的饱和溶液的溶质的质量分数一定大于其不饱和溶液的溶质的质量分数
④t3℃时,将甲、乙、丙三种物质溶液恒温蒸发相同质量的水,析出晶体质量大小关系为甲>乙=丙

试回答:


【实验目的】探究试管中溶液的中和反应程度
【做出猜想】猜想1:氢氧化钠未完全反应,溶液呈碱性;猜想2:氢氧化钠和盐酸恰好完全反应,溶液呈中性;猜想3:氢氧化钠完全反应、盐酸过量,溶液呈酸性
实验操作 | 实验现象 | 实验结论 |
另用试管取该溶液1~2 | 溶液变 | 溶液呈碱性 |
溶液不变色 | 溶液呈 |
方案1 | 用 |
方案2 | 加入碳酸钙粉末,若有产生,则溶液呈酸性 |

【提出问题】久置氢氧化钠固体的成分是什么?
实验方案 | 实验现象 | 结论及解释 |
方案一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸。 | 实验过程中始终没有气泡产生。 | 则证明猜想成立 |
方案二:另取固体样品于试管中,加蒸馏水完全溶解,然后滴加少许氯化钡溶液。 | 实验过程中产生 | 则证明猜想二或三成立。 |

①800s时,曲线a表示的溶液显(填“酸”或“碱”)性
②通过对比曲线a和曲线b(填“不能”或“能”)证明NaOH与CO2发生了化学反应,理由是。
