 水力发电
C .
水力发电
C .  汽车燃油做功
D .
汽车燃油做功
D .  火箭点火升空
火箭点火升空

 B . 滴加蒸馏水
B . 滴加蒸馏水  C . 振荡土壤液
C . 振荡土壤液 D . 测定酸碱性
D . 测定酸碱性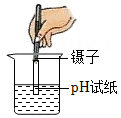




|
选项 |
结构 |
性质, |
用途 |
|
A |
碳酸钙中含有碳酸根离子 |
与酸反应 |
制取二氧化碳 |
|
B |
氢氧化钙溶液含有氢氧根离子 |
具有碱性 |
中和酸性土壤 |
|
C |
一氧化碳含有碳元素 |
有可燃性 |
用于炼铁 |
|
D |
硫酸中含有氢离子 |
具有酸性 |
金属除锈 |






甲:KCl、K2CO3、CaCl2 , 乙:KNO3、Ca(NO3)2、KCl
序号 | 评价标准 | 分值 |
1 | 营养液中含N、P、K元素,每一种可加1分(同种只加1分) | 3分 |
2 | 组内物质均能共存,不发生化学反应,发生一个扣1分 | 2分 |

实验一:通过溶液酸碱度证明酸碱发生中和反应,图②中b、c、d三点处对应溶液所含溶质NaCl的质量大小关系(用b、c、d表示三者关系)。
实验二:③④⑤操作,(选填“可以”或“不可以”)证明酸与碱发生了中和反应。








【查阅资料】部分氢氧化物形成沉淀时所对应的溶液pH值,如表所示。
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀时溶液的pH值 | 1.9 | 4.2 | 9.1 |
完全沉淀时溶液的pH值 | 3.2 | 6.7 | 11.1 |
①氯化钠 ②碳酸钠 ③碳酸钡 ④稀盐酸

【实验探究】实验结束后,小江同学将试管丙中物质过滤,把所得滤液与试管丁中的溶液倒入一个干净的烧杯中混合,过一会儿先有气泡冒出,后有白色沉淀生成,从而确定混合前试管丁中溶液的溶质是(填化学式)。
【提出问题】混合后烧杯中溶液的溶质成分是什么?
【进行猜想】猜想一:NaCl;猜想二:NaCl、Na2CO3;猜想三:。
【设计实验】
实验步骤 | 实验现象 | 实验结论 |
取少量烧杯中的混合溶液于试管中,加入碳酸钠溶液。 | ▲ 。 | 猜想三成立 |
上述表格空格处填空

| 石块的体积/厘米3 | 弹簧秤的示数/牛 | OB的长度 | OA的长度 |
物体处于空气中 | 150 | 1.8 | 30 | 10 |
物体浸没在液体中 | 150 | 1.2 | 30 | 10 |
实验 序号 | 铁粉 (克) | 氧化铜 (克) | 9.8%稀 硫酸(克) | 实验现象 |
1 | 0.56 | 1.6 | 60 | 立即出现红色固体,无气泡产生,充分反应后上层清液呈蓝色 |
2 | 1.68 | 1.6 | 60 | 立即出现红色固体,待红色固体不再增加后产生大量的气泡,充分反应后上层清液呈浅绿色 |
铁粉、氧化铜的混合物与稀硫酸,能发生如下反应:
①Fe+H2SO4═FeSO4+H2↑;②氧化铜与稀硫酸反应;
③Fe+CuSO4═FeSO4+Cu。



材料1:如图所示为我国科学家研发的循环制氢和贮存氢气的新工艺。

材料2:为了促进氢能利用,科学家设计了如图所示的人工光合作用系统,模拟植物利用太阳能合成糖类的过程。
