
选项 | ① | ② | ③ | 装置Ⅱ中实验现象 |
A | 浓氨水 | 氧化钙 | 硫酸铝溶液 | 先产生白色沉淀,后沉淀溶解得到澄清溶液 |
B | 稀硫酸 | CuS | 新制氯水 | 产生乳黄色沉淀 |
C | 浓硫酸 | Cu | 石蕊溶液 | 先变红,后褪色 |
D | 稀硫酸 | 碳酸钠 | 饱和碳酸钠溶液 | 产生白色沉淀 |

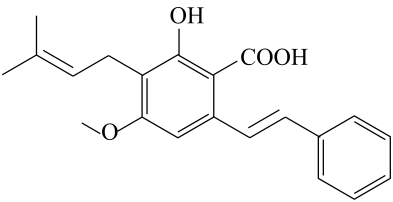

[查阅资料]
①
②极易溶于水而不与水反应,几乎不发生水解,沸点11℃。
③饱和溶液在低于38℃时析出
, 高于38℃时析出
, 高于60℃时
分解成
和NaCl。

准确称取mg的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: , 将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液作指示剂,用
标准液滴定至终点,测的标准溶液体积的平均值为VmL(已知
)
①确认滴定终点的现象是。
②所称取的样品中的质量分数为(用含c、V的代数式表示)。

已知:①P2O4为磷酸酯萃取剂;②Sc3+易水解;③Ksp[Sc(OH)3]=8.00×10-31。
请回答下列问题:
试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
1-1 | 1 | 分相快 | 90.76 | 15.82 |
1-2 | 2 | 分相容易 | 91.53 | 19.23 |
1-3 | 3 | 分相容易 | 92.98 | 13.56 |
1-4 | 4 | 有第三相 | 90.69 | 30.12 |
1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |

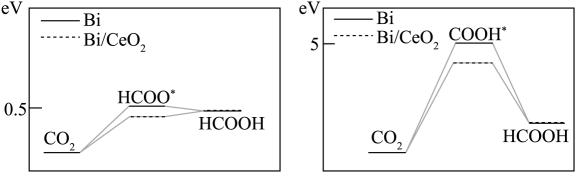
反应i. CO2(g)+H2(g) HCOOH(g) ΔH1
反应ii. CO2(g)+H2(g) H2O(g)+CO(g) ΔH2>0
反应iii.……
可能的反应机理如下(M为催化剂);
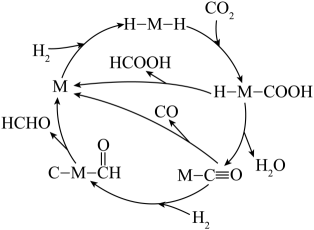
回答下列问题:
物质 | CO2(g) | H2(g) | HCOOH(g) |
标准摩尔生成焓/kJ·mol-1 | -393.51 | 0 | -362.3 |
依据以上信息,ΔH1=。

①下列措施能提高CO2平衡转化率的是 ( 填标号)。
A.降低温度 B.再充入Ar C.分离出HCOOH
②673.15K,反应后体系中H2的分压为a MPa,则反应i的压力商计算式Qp= MPa-1。
③当温度高于673.15K,随温度升高,反应i与反应ii的反应速率相比,增加更显著的是反应 (填“ i”或“ii”),判断的理由是。

化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
熔点/℃ | 377 | -24.12 | 38.3 | 155 |


a.几何因素 b.电荷因素 c.键性因素

已知以下信息:
①
R1CHO+

②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
⑤RNH2+
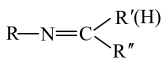 +H2O
+H2O
回答下列问题:

反应条件1所选用的试剂为,反应条件2所选用的试剂为,I的结构简式为。