|
|
|
|
A.白糖 | B.食盐 | C.辣椒 | D.大蒜 |
 )存在顺反异构体
B . 对苯二甲酸(
)存在顺反异构体
B . 对苯二甲酸( )属于芳香烃
C . 雪花
)属于芳香烃
C . 雪花 D . 基态
D . 基态
选项 | 生产生活 | 化学原理 |
A | 焊接金属时用 |
|
B |
|
|
C |
|
|
D | 酿制葡萄酒过程中添加适量二氧化硫 | 二氧化硫有还原性和杀菌作用 |
|
|
|
|
A.制备 | B.干燥 | C.收集 | D.尾气处理 |

选项 | 实验操作 | 离子方程式 |
A | 将 |
|
B | 向草酸溶液中滴加几滴酸性 | |
C | 实验室电解饱和食盐水生成黄绿色气体 | |
D | 酚酞滴入醋酸钠溶液变为浅红色 |
选项 | 操作 | 现象 | 结论 |
A | 向 | 溶液不变色 |
|
B | 向待测液中滴加 | 生成蓝色沉淀 | 溶液中有 |
C | 向 | 先生成蓝色沉淀,然后沉淀溶解 |
|
D | 向酸性 | 溶液紫红色变浅 | 乙醇被还原生成乙酸 |
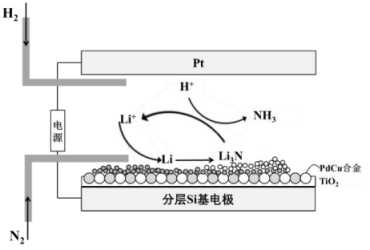
Ⅰ.实验准备:饱和氯水的制备
①取溶液于试管中,滴加3滴
溶液,溶液变红色;
②取溶液于试管中,先滴加3滴
溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
【发现问题】小组成员针对实验②中溶液未变红色,而呈现黄色的现象展开了探究。
【查阅文献】
i.能将
氧化成
, 硫氰
常温下为黄色液体,易挥发,可与水发生反应:
;
ii. ,
为无色配合物。
【提出猜想】猜想一 被氯水氧化成
, 使溶液呈黄色;
猜想二 加入氯水后部分被氧化为
,
(红色),但由于存在反应:
, 实验②生成的
浓度比实验①的小,
溶液在浓度较低时呈黄色。
【验证猜想】为验证猜想,小组成员设计了以下实验,请补充表格中的操作及现象
实验序号 | 实验操作 | 现象 | 实验结论 |
③ | 取少量实验①的溶液于试管中, | 猜想二正确 | |
④ | 取少量实验②的溶液于试管中,滴加3滴饱和 | 溶液变浑浊 | 猜想一也正确 |
| 实验序号 | 实验操作 | 现象 |
⑤ | 滴加3滴蒸馏水 | 无明显现象 | |
⑥ | 滴加3滴饱和氯水 | 无明显现象 | |
⑦ | 溶液变橙红色 | ||
⑧ | 滴加3滴 | ||
得出结论 | i.由实验⑥的现象可以判断:猜想一不正确, ii.结合实验⑤⑦⑧的现象可以判断:猜想二正确。 | ||

已知:①25℃时,相关金属离子形成氢氧化物沉淀的
范围如下:
金属离子 | |||||
开始沉淀的 | 6.3 | 1.8 | 3.4 | 6.9 | 7.1 |
沉淀完全的 | 8.3 | 3.2 | 4.7 | 8.9 | 9.1 |
②氧化前后,溶液中、
元素的化合价均为+2价。

已知:溶液吸光度大小与溶液颜色深浅成正比。
①基态原子的核外电子排布式:。
②完成离子方程式:
实验①:向一定量待测溶液中滴加过量酸性
溶液,振荡后加入过量的淀粉-KI溶液。
实验②:用等体积去离子水代替实验①中的溶液,重复上述操作。
两组实验充分反应后,测得不同波长下吸光度 , 绘制吸收光谱曲线如下图所示。

①请你判断表现实验①中溶液吸光度的曲线为。
②根据上图曲线,选定在波长下,测定不同浓度
溶液的吸光度
, 得到
之间的关系为:
。
, 某待测溶液的吸光度
为0.182,则该溶液中
含量为
。
已知反应a:
反应b:
反应c:
反应d:
。

①600℃时,体系中的物质的量为
,
平均反应速率
。
②当温度高于650℃,甲醛的选择性下降的原因不可能是。
A.升高温度使催化剂活性降低 B.升高温度使反应逆向移动
C.温度升高反应速率加快 D.升高温度使反应
正向移动
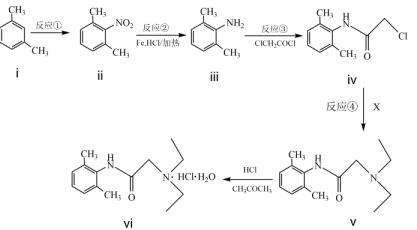
序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
a | 加成反应 | ||
b | 氧化反应(生成有机产物) |
 。
。已知 。
。
基于你设计的合成路线,回答下列问题:
(a)合成路线中,填(“有”或“没有”)涉及到碳原子杂化类型的改变。
(b)步骤中涉及反应④原理的化学方程式为。