选项 | 物质 | 性质 | 用途 |
A. | ClO2 | 强氧化性 | 自来水消毒剂 |
B. | Fe2O3 | 红色 | 油漆中的红色颜料 |
C. | Na2CO3 | 水解显碱性 | 治疗胃酸的药物成分 |
D. | 钛合金 | 耐高温、耐腐蚀 | 制做发动机的火花塞 |
选项 | 探究方案 | 探究目的 |
A | 向2mL 0.1mol/L KI溶液中加入5mL 0.1mol/L | 化学反应有一定限度 |
B | 用玻璃棒蘸取待测溶液滴在pH试纸上,立即与pH标准比色卡对照读数 | 测定新制氯水的pH |
C | 分别向2支盛有等体积、等浓度的 | 探究不同催化剂对反应速率的影响 |
D | 分别取50mL 0.5mol/L硫酸、氢氧化钠两溶液在量热器中充分反应,测定反应前后最大温度差 | 测定中和热 |
选项 | 操作 | 现象 | 结论 |
A | 在常温下测定Na2CO3和NaHCO3溶液的pH | Na2CO3溶液pH较大 | 水解能力:Na2CO3大于NaHCO3 |
B | 先向盛有1mL 0.1mol/L的AgNO3溶液的试管中滴加两滴0.1mol/L的NaCl溶液,再向其中滴加0.1mol/L的NaI溶液。 | 滴加NaCl溶液有白色沉淀生成,滴加NaI溶液后有黄色沉淀生成 | AgCl沉淀可转化成AgI沉淀 |
C | 电解饱和CuCl2溶液实验中,用润湿的淀粉—碘化钾试纸靠近阳极 | 润湿的淀粉—碘化钾试纸变蓝 | 阳极产生Cl2 |
D | 饱和FeCl3溶液中加入少量NaCl固体 | 溶液颜色变浅 | 加入NaCl固体后,FeCl3的水解平衡逆向移动 |
实验 | 操作 | 现象 |
Ⅰ |
| 10h后,铜片表面附着黑色固体 |
Ⅱ |
| 立即产生大量气泡,溶液变为浅蓝色,铜表面光洁 |
Ⅲ |
| 立即产生大量气泡,溶液蓝色较深,铜片依然保持光亮 |
下列说法错误的是( )

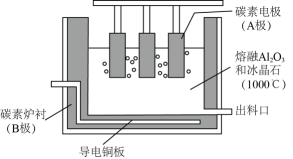
已知“焙烧”过程中的主反应为:
Mg3(Si2O5)(OH)4+5(NH4)2SO4![]() 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
a. NaOH b.Ca(OH)2 c.NH3·H2O
t/min | 2 | 4 | 7 | 9 |
n(I2)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
请回答:
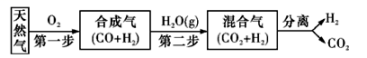
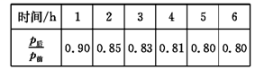
①用H2表示的前2h的平均反应速率v(H2)=
②该温度下,CO2的平衡转化率为
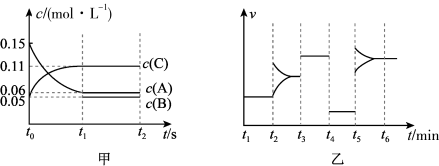
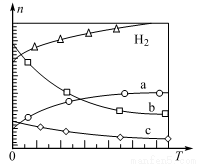
①该反应的△H0(填“>”或“<”)。
②曲线表示的物质为(填化学式)。
【实验原理及方案】在酸性溶液中,碘酸钾和亚硫酸钠可发生反应生成碘,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
实验序号 |
|
| 水的体积/mL | 实验温度/℃ | 记录出现蓝色的时间/s |
① | 5 | 5 | 0 | ||
② | 5 | 5 | 40 | 25 | |
③ | 5 | 35 | 25 |
【实验步骤】ⅰ.向溶液中滴加5~6滴
溶液,充分反应后,将所得溶液分成甲、乙两等份;
ⅱ.向甲中滴加 , 充分振荡;
ⅲ.向乙中滴加溶液。
证明反应存在一定限度的实验现象是:步骤ⅱ中;步骤ⅲ中。
实验三:测定反应的平衡常数K
常温下,取2个碘量瓶分别加入下表中的试剂,振荡半小时。取一定体积的上层清液用标准溶液进行滴定,测定
和
的总浓度。
编号 |
|
|
试剂 |
|
|
|