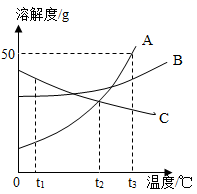
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是。
②当温度在t2~t3℃之间时,A物质与B物质(填“能”或“不能”)配制溶质质量分数相同的饱和溶液。
③将A、B、C三种物质的饱和溶液分别由t2℃升温到t3℃,所得溶液中溶质的质量分数最大的物质是。
④t3℃时将75gA的饱和溶液稀释成20%的溶液需加g水。
①用量筒量取水时,俯视读数 ②试剂、砝码的左右位置颠倒且使用游码
③用量筒量取水时,仰视读数 ④用于溶解的烧杯中有少量的蒸馏水
⑤转移溶液时有部分液体溅出
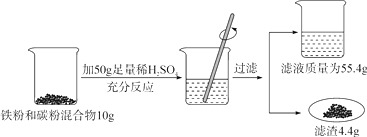
Ⅰ.我国海盐年产量3 千多万吨,居世界第一位,目前从海水中提取食盐的方法主要为“盐田法”,生产流程如下:

①潮汐能 ②生物能 ③电能 ④太阳能 ⑤化学能
Ⅱ.金属镁广泛应用于生活、生产和国防工业.从卤水中提取镁的过程所示:
![]()
在上述转化过程中,②处发生的化学方程式是;属于基本反应类型的反应.

①图中曲线交点表示的含义是.
②t1℃时,KCl 饱和溶液的溶质质量分数KNO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一).
③已知20℃时,KNO3 的溶解度为31.6g;80℃时,KNO3的溶解度为169g.在20℃时,向盛有200g 水的烧杯中加入80g 硝酸钾,充分溶解,得到该温度时KNO3 的(填“饱和”或“不饱和”)溶液,若使烧杯内物质缓慢升温至80℃,(忽略水分蒸发) 在该温度下,最后所得溶液中溶质与溶剂的质量之比为(填最简整数比).
④若KNO3溶液中混有少量的NaCl 杂质,可以采取方法获得较纯净的KNO3 .
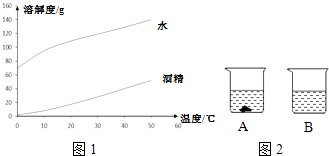
表一 甲、乙分别在水、酒精中的溶解度
甲 | 乙 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
图2 甲分别在水、酒精中的溶解度曲线
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.