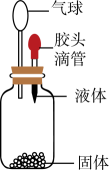
选项 | 固体 | 液体 |
A | 二氧化锰 | 过氧化氢溶液 |
B | 生石灰 | 水 |
C | 硝酸铵固体 | 水 |
D | 碳酸钠粉末 | 稀硫酸 |
所加溶液 | 甲 | 乙 | 丙 |
实验现象 | 产生白色沉淀 | 产生蓝色沉淀 | 无明显现象 |
| 物质 | 杂质 | 除杂方案 |
A | 铜粉 | 氧化铜 | 在空气中充分灼烧 |
B | CO2 | CO | 向其中通入过量氧气,点燃 |
C | NaCl固体 | 细沙 | 加入足量水溶解,过滤,蒸发结晶 |
D | Na2SO4溶液 | NaOH | 滴加适量的稀盐酸 |
![]()
②一种不稳定的酸。
③一种难溶于水的碱。
④一种易溶于水的盐。
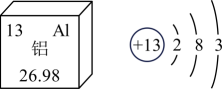
淀粉[主要成分为(C6H10O5)n]是面粉的成分之一,淀粉是由种元素组成的,淀粉中碳元素与氧元素的质量比为(填最简整数比)。芝麻中富含的钙和磷等矿物质,对于骨骼的生长和骨密度的维持具有重要作用。通常情况下,芝麻含“钙”量大约是每100克含钙量在200毫克左右。这里的“钙”指的是(选填“元素”“单质”“分子”之一)。
②日日扁舟藕花里,有心长作济南人。部分莲藕因所开的莲花为白色,被称作“白莲藕”,色泽洁白如玉,口感鲜嫩脆。莲藕中含有大量的维生素C和植物膳食纤维,营养丰富。维生素C(化学式:C6H8O6)中质量分数最大的元素是(填元素符号)。
③催泪无心因味激,入喉有意慰肠鸣。“皮牙子”是新疆人对洋葱的称呼。洋葱中含有一种具有强烈刺激性气味的物质一正丙硫醇(CH3CH2CH2SH)。一个正丙硫醇分子中氢原子与碳原子的个数比为(填最简整数比)。请从微观角度解释,切圆葱时人们常被刺激的流眼泪的原因:。
②风雪过后,大型铲雪车日夜轰鸣。铲雪车的铲斗是用锰钢制造的,其中至少含有锰、碳、铁、铬等元素,同时也说明了合金与组成它的纯金属相比,优点之一是硬度(填“大”或“小”)。
③为防止道路结冰,雪后可向路面撒融雪剂。融雪剂有多种,一类是以醋酸钾(CH3COOK)为主要成分的有机融雪剂。196g醋酸钾(CH3COOK)中含碳元素的质量为g。
④乙酸钾可由氢氧化钾或碳酸钾与乙酸发生化学反应制备:2CH3COOH+K2CO3=2CH3COOK+CO2↑+X,则X的化学式为;
⑤环保型的融雪剂多为不含或少含MgCl2、CaCl2的混合物,不合理使用上述含钙、镁化合物的融雪剂的危害是(选填“A、B或C”之一)
A.产生污染性气体 B.使水质硬化 C.难以溶解,不便于清理

①t1℃时,向50g水中加入25g NH4Cl固体,经搅拌充分溶解,所得溶液中溶质与溶剂的质量之比为(填最简整数比)。
②在t2℃时,KNO3的溶解度NH4Cl的溶解度(选填“大于”“等于”“小子”之一)。
③t2℃时,KNO3饱和溶液中溶质的质量分数是(计算结果精确至0.1%)。
④t2℃时,分别将KNO3和NH4Cl两物质的饱和溶液降温至t1℃,降温后两溶液中所含溶质质量大小关系为AB(选填“大于”、“小于”、“等于”或“不能确定”)。
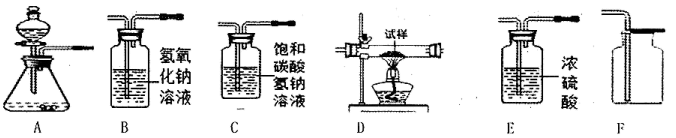
①所选仪器的连接顺序为(从左到右填写仪器序号字母)。
②上述制二氧化碳的化学方程式为。
③下列有关叙述中,正确的是(选填“A、B、C或D”之一)。
A.在制取氧气反应前后,MnO2的质量和性质都不发生改变
B.二氧化碳含量过高可导致缺氧窒息,是因为二氧化碳有毒
C.用向上排空气法收集二氧化碳时,把燃着的小木条放到集气瓶口,可检验是否收集满
D.因红磷和木炭均可和氧气发生化学反应,所以都能用于“测定空气中氧气含量”实验
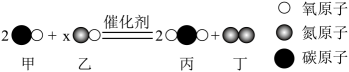
①A中发生的化学反应方程式为。
②实验时,观察到装置D中的现象为
③若去掉装置E3(其他不改变),充分反应后,仍然使用E2浓硫酸洗气瓶的质量增加计算氧化铜的质量,则计算结果将(填“不受影响”、“偏大”或“偏小”)。
④若充分反应后,装置D质量减少了ag,则试样中氧化铜的质量为g(用含a的式子表示,下同),装置E2的质量变化为g。
②小红从下列四种试剂中选取了一种试剂,进行鉴别实验,根据明显现象也成功鉴别了上述两种无色溶液。则小红所选的这种试剂是(填选项序号之一)。
A.紫色石蕊溶液 B.稀盐酸 C.K2CO3溶液 D.NaNO3溶液

试根据实验过程和图示提供的信息,进行分析推理,回答下列问题:
①无色气体B的水溶液pH7(选填“大于”、“小于”或“等于”);
②白色沉淀G的化学式为;
③无色滤液F中存在的阴离子为(写离子符号);
④根据上述实验现象推断,在固体混合物A里,上述四种物质中,肯定不存在的物质是(填化学式),理由是。

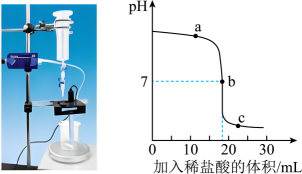
①当滴入NaOH溶液120g时(即图中B点),烧杯中溶液里含有的溶质为(写化学式);
②当滴入10%的NaOH溶液80g时(即图中A点),恰好完全反应。试通过计算,求10g此氯化镁样品中MgCl2的质量。(计算结果精确至0.1g)