




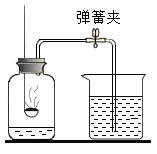
| 实验操作 | 现象 | 结论 |
A | 在带尖嘴的导管口点燃某气体,然后在火焰上方罩一冷而干燥的小烧杯 | 烧杯内壁有水雾 | 该气体不一定是H2 |
B | 把硫在空气中点燃,再伸进充满氧气的集气瓶里 | 硫在空气中燃烧发出淡蓝色火焰,在氧气中燃烧发出蓝紫色火焰 | 硫在空气中燃烧生成SO2 , 在氧气中燃烧生成SO3 |
C | 将用石蕊溶液染成紫色的湿润的纸花放入盛满二氧化碳的集气瓶中 | 纸花变为红色 | 使石蕊变红的物质为二氧化碳 |
D | 称量铜粉在空气中加热前后的质量 | 加热后的质量比原来铜粉的质量大 | 该化学反应不遵循质量守恒定律 |

①绿色植物通过吸收CO2。
②风化的岩石(主要成分:CaCO3)粉来吸收空气中的CO2和H2O,发生化合反应后生成Ca(HCO3)2 , 该反应的化学方程式为。
①从微观角度分析,二氧化碳被压缩过程中变化的是。
②下列对超临界二氧化碳的理解正确的是(填字母)。
A.超临界二氧化碳与二氧化碳的组成元素不同
B.超临界二氧化碳容易燃烧
C.超临界二氧化碳存在于特定的条件下,条件改变,状态改变

①该转化中循环利用的物质有Fe3O4和(填化学式);
②与电解水相比,该方法的优点是。
③CH4-H2O催化重整是目前大规模制取H2的重要方法,生产过程中涉及的重要反应有:CH4+H2OCO+3H2 , CO+H2O
CO2+H2。向催化重整体系中投入一定量的CaO可吸收二氧化碳,从而提高H的百分含量,如图乙所示,投入纳米CaO时,H2的百分含量最大,其原因是。
可燃冰外观类似冰,主要含甲烷水合物【由甲烷(CH4)分子和水分子组成】,还含少量二氧化碳等气体。甲烷水合物的分子结构就像一个个由若干水分子组成的笼子。每个笼子里“关”一个甲烷分子。温度不高、压力足够大、有甲烷气源时甲烷可与水生成甲烷水合物,分散在海底岩层的空隙中。甲烷水合物能稳定存在的压强和温度范围如图所示。

1体积可燃冰可储载约164体积的甲烷气体。可燃冰储量丰富,燃烧热值大,因而被各国视为未来石油天然气的替代能源。甲烷还是重要的化工原料,可制造炭黑、乙炔、氰化氢等。由甲烷引发的温室效应比二氧化碳厉害10至20倍。可燃冰一旦离开海床便迅速分解,容易发生喷井意外,还可能会破坏地壳稳定平衡,引发海底塌方,导致大规模海啸。所以可燃冰的开采难度较大。

图1所示反应的化学方程式为;在图2横线处补全相应微粒的图示。

①A点对应的物质类别是。B点表示物质的化学式为,写出该物质与氧化铜反应的化学方程式。
②写出由C点表示的物质与水发生反应生成碳酸的化学方程式;写出由C点表示的物质转化为B点表示的物质的化学方程式。

写出乙瓶中发生反应的化学方程式,振荡后,甲、乙、丙中气体压强由大到小的顺序是;仿照乙画出此时甲中气体组成的微观示意图。
药品 | 实验编号 | |||
甲 | 乙 | 丙 | 丁 | |
大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
【查阅资料】
①同温度同压强下,气体的体积与气体所含分子数成正比;
②同温度同压强下,任何气体的分子间距几乎均相等;
③在常温常压下,相同分子数的任何气体的体积几乎相等。

瓶B与瓶C中,以下相同的是____。

定性检测:
实验操作 | 实验现象 | 实验结论 |
连接装置,检查气密性,装入试剂并按上图进行实验。通入O2 , 一段时间后,点燃J处酒精灯。 | 装置K中无水CuSO4变色 | 塑料燃烧产物中有H2O |
装置L中。 | 塑料燃烧产物中有CO2 |
由上述实验可得出结论:该塑料一定含有的元素是(填元素符号)。