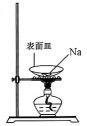
 钠的燃烧
B .
钠的燃烧
B . 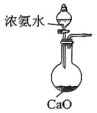 用浓氨水和
用浓氨水和 蒸发
蒸发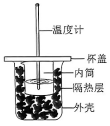 测定中和反应的反应热
测定中和反应的反应热
再加入粒,溶液颜色加深。
振荡,一段时间后,紫黑色晶体消失,且溶液褪色。
下列实验现象对应的解释正确的是( )。
选项 | 实验步骤及其现象 | 解释 | |
A | 溶液呈浅棕色 |
| |
B | 溶液颜色加深 | 因Zn与 | |
C | 紫黑色晶体消失 | Zn参与反应,促使体系中 | |
D | 溶液褪色 | 因 | |
①基态X原子的核外电子排布式为。
②写出一项比较Rb与Z的金属性强弱的方法:。

①晶胞中含有的个数为。
②该晶胞密度为(设阿伏加德罗常数的值为
, 用含a的代数式表示)。
ⅰ.将粗品溶于盐酸,作电解槽的阳极液;
溶液做阴极液,两者用离子交换膜隔开,用惰性电极电解:
ⅱ.向溶液中加入少量
溶液并共热,过滤、洗涤、干燥得纯品
。
①写出步骤ⅰ阳极的电极反应式:;离子交换膜宜选用(填“阳离子交换膜”或“阴离子交换膜”)。
②步骤ⅱ加热条件下生成沉淀的离子方程式是。
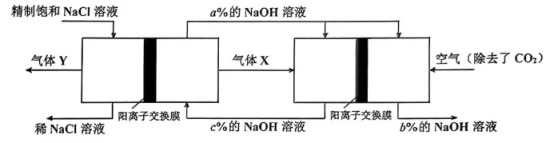
M(电解池) N(燃料电池)
①气体X在N池中反应的电极方程式为。
②图中气体Y的化学式为;M池所用的离子交换膜允许通过的主要离子有。
③图中三处溶液的质量分数由大到小的顺序为。
④写出一项此流程设计的优点:。
写出该反应的化学方程式:。
用离子方程式及化学平衡移动原理解释上述变化:。
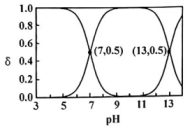
①写出的电离方程式:、。
②的
,
。
ⅰ.
ⅱ.
①反应ⅰ能自发进行的反应条件是。
②写出热解总反应的热化学方程式:。
③假设在某温度下反应ⅰ达到平衡,测得密闭系统中各组分浓度分别为、
、
。
该温度下平衡常数;达平衡后,其他条件不变,把容器的容积减小到原来的
时,结合数据用Q与K的大小关系解释平衡移动方向及其理由。
①先将通入
溶液中,产生淡黄色沉淀和浅绿色溶液(已知
是黑色难溶物)。写出该反应的离子方程式:。
②再在硫杆菌存在下通入:
在硫杆菌存在下被氧化的速率是无菌时的
倍。
ⅰ.硫杆菌的作用是;
ⅱ.由下图1和图2判断使用硫杆菌的最佳条件为;

图1 图2
ⅲ.若反应温度过高,反应速率下降,其原因是。
B在乙醇溶液加热条件下反应的有机产物的结构简式为;欲检验B中含有的溴原子,可在上述反应后的溶液中依次加入的试剂为。
①可发生银镜反应
②碳骨架没有支链
③能与
溶液反应
写出其中核磁共振氢谱有吸收峰面积比为的结构简式:。