 单质
B .
单质
B . 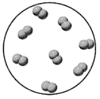 化合物
C .
化合物
C . 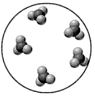 化合物
D .
化合物
D .  混合物
混合物
 取用粗盐
B .
取用粗盐
B .  加热液体
D .
加热液体
D .  连接仪器
连接仪器



实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸以及下列仪器: 
查阅资料:蚁酸化学名称为甲酸(),熔点为8.6℃,一定条件下加热分解生成两种物质;
常温下氯化钯()溶液常用于检验
的存在:
。
探究Ⅰ:蚁酸的分解产物

探究Ⅱ:产物的性质

①【查阅资料】镍能与稀硫酸反应生成能溶于水的 , 并放出氢气。写出镍与稀硫酸反应的化学方程式;
②【猜想与假设】根据教材中常见金属的活动性顺序和查阅的资料,对以上三种金属的活动性做出猜想:猜想①;猜想②;
③【实验探究】把用砂纸打磨过的镍片浸入中,过一会取出,发现镍片表面无明显变化。证明(填“猜想①”或“猜想②”)成立;
④【拓展延伸】用铜片、溶液和,通过实验探究也能判断
、
、
的金属活动性顺序。