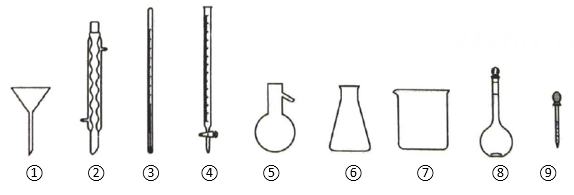
元素代号 | 元素的性质或原子结构 |
Q | 有一种原子不含中子 |
W | M层上的电子数为4 |
X | 常温下单质为双原子分子,其简单氢化物的水溶液显碱性 |
Y | L层的电子数为次外层电子数的3倍 |
Z | 元素的最高化合价是 |
下列叙述中错误的是( )
选项 | 实验操作 | 现象 | 结论或解释 |
A | 向 | 溶液变红 |
|
B | 常温下,测定等浓度的 | 前者大于后者 | 非金属性: |
C | 将某溶液滴在 | 试纸变蓝 | 原溶液中一定含有 |
D | 向蛋白质溶液中加入醋酸铅溶液 | 产生白色沉淀 | 蛋白质发生了盐析 |
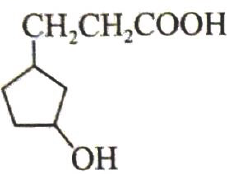 的分子式为
的分子式为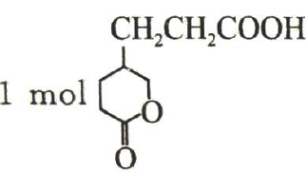 最多可与
最多可与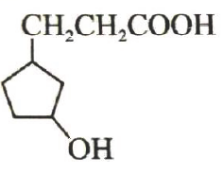 含有两种官能团
含有两种官能团
【实验原理】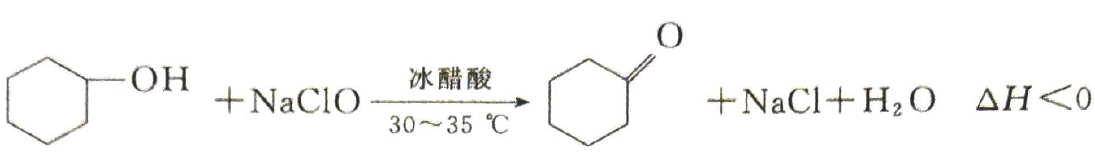 .
.
【装置示意图】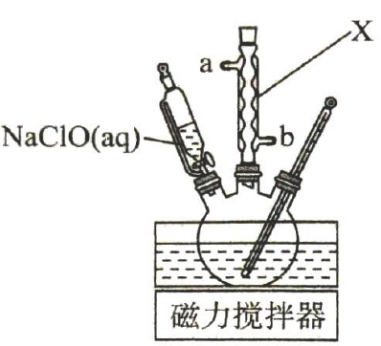
【实验步骤】Ⅰ.烧瓶中依次加入环已醇和
冰醋酸,开动磁力搅拌器.在冰水浴冷却下,逐滴加入次氯酸钠溶液至稍过量.
Ⅱ.在室温下继续搅拌 , 然后加入饱和亚硫酸氢钠溶液.
Ⅲ.在反应混合物中加入水、
氯化铝,去掉仪器X,换成蒸馏装置,加热蒸馏,至馏出液无油珠滴出为止.
Ⅳ.在搅拌情况下向馏出液中加入无水碳酸钠至中性,然后再加入精制食盐使之饱和,将此液体倒入分液漏斗,分出有机层.
Ⅴ.向有机层中加入无水 , 静置,过滤,对滤液进行蒸馏,得到产品
.
回答下列问题.
用淀粉碘化钾试纸可检验反应后的液体,如果试纸变色,说明次氯酸钠过量.
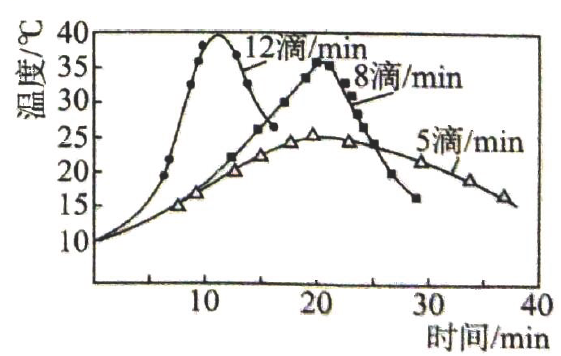
物质 | ||
相对能量/ |
步骤1 步骤2 步骤3
①写出步骤1反应的离子方程式:.
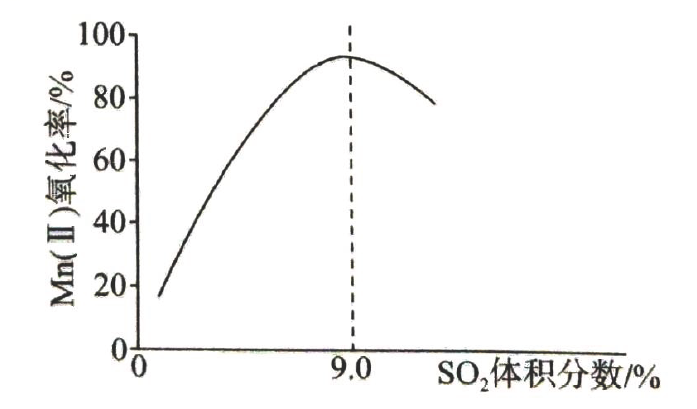
②其他条件不变,步骤1中转化为
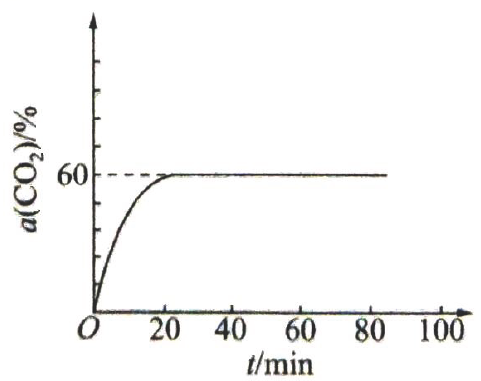
的转化率与温度的关系如图所示.
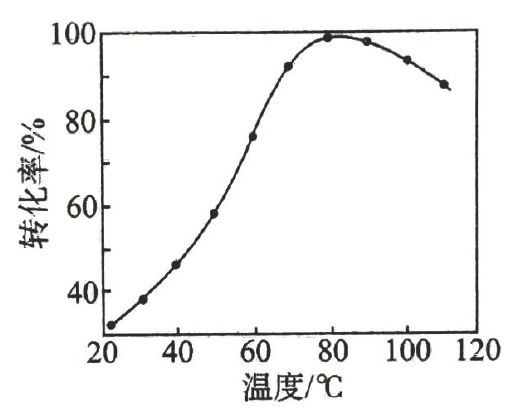
步骤1的转化率开始迅速上升,主要原因是,后又下降的可能原因是.
③流程图步骤2中,加入乙醚的作用是,步骤3的分离方法是.
已知平衡后,测得 , 则反应Ⅰ的
(用含
的式子表示).
①能与金属钠反应产生氢气;②在铜催化氧化的条件下,氧化产物能发生银镜反应.其中,核磁共振氢谱显示为3组峰,且峰面积比为的同分异构体的结构简式为.
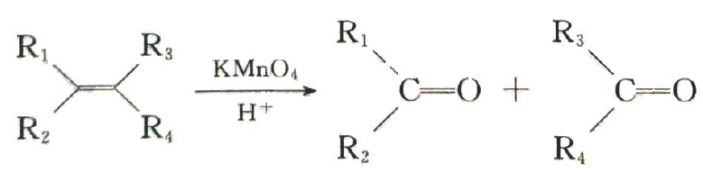 , E与足量酸性
, E与足量酸性