
 氯化钠
B .
氯化钠
B .  红磷
C .
红磷
C .  硫酸
D .
硫酸
D .  酒精
酒精

| 实验操作 | 现象 | 结论 |
A | 某待测液中加氯化钙溶液 | 有白色沉淀生成 | 该溶液为AgNO3溶液 |
B | 将CO通入氧化铁粉末中 | 粉末由黑色变为红色 | CO有还原性 |
C | 将2根铜丝分别放入硫酸铝溶液和硝酸银溶液中,观察现象 | 硫酸铝溶液没有明显现象,硝酸银溶液逐渐变蓝,其中铜丝表面有银色物质析出 | 金属活动性顺序:Al>Cu>Ag |
D | 将铜片和黄铜片相互刻画 | 铜片上留下划痕,黄铜片无明显现象 | 合金硬度比组成它的纯金属硬度小 |
新能源汽车已经走进了我们的生活。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。
I.电动汽车
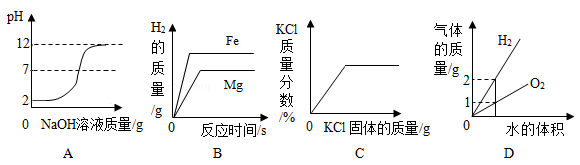
电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示。其中能量密度表示单位体积的电池所具有的能量。

Ⅱ.氢内燃车
氢内燃车以氢气为燃料,不排放任何污染物。氢气可通过电解水(原理如图2)等多种方式获得。据测算,1kg氢气完全燃烧可释放14.3×104kJ的热量,1kg汽油完全燃烧可释放4.6×104kJ的热量。

Ⅲ.乙醇汽车
乙醇汽东车乙醇为燃料。乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取。
我国新能源汽车发展迅速,未来可期。

实验组别 | 实验条件 | 试管 A 中的现象 | 试管 B 中的现象 |
甲 | 未加热 | 固体无变化 | 无明显现象 |
乙 | 酒精灯加热 | 固体部分溶解 | 呈浅红色 |
丙 | 酒精喷灯加热 | 固体部分溶解 | 呈红色 |

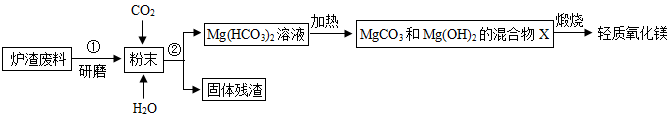
【查阅资料】Mg(OH)2、MgCO3受热易分解,分解温度不同,各生成对应的两种氧化物。请根据流程图回答下列问题:

①BC段的固体成分是。
②写出C点中固体发生反应的化学方程式。
③混合物X中MgCO3和Mg(OH)2的质量比是,若混合物X用aMgCO3·bMg(OH)2表示,a:b=。
Pb | |||
单质 | 氧化物 | 碱 | 硝酸盐 |
方案 | 预期反应的化学方程式 | 依据的反应规律 |
① | 。 | 盐+盐→新盐+新盐 |
② | 。 | (略) |
③ | 。 | (略) |
①写出加热高锰酸钾制取氧气的化学方程式。
②实验方案:取相同质量的氯酸钾和高锰酸钾(需要催化剂的加入适量催化剂),用排水法收集氧气,比较相同时间内产生氧气体积的多少。
请从下图中选择合适的仪器(每种仪器限用一次)进行完整的探究实验,不需要用到的是(填标号)。

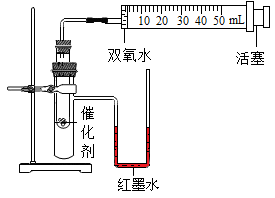
实验序号 | 过氧化氢溶液 | 催化剂 |
实验1 | 5mL4% | 粉末状MnO2 0.2g |
实验2 | 5mL4% | 粉末状CuO 0.2g |
①实验2中制取氧气的化学方程式为。
②实验需要测量并记录的数据有:氧气体积和。
③实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U型管内右侧液面上升,原因是。(填字母)
a.过氧化氢分解产生氧气,使装置内压强变大
b.过氧化氢分解放热,使装置内气体膨胀,压强变大
④结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是。
a.取少量粉末于研钵中研磨,扇闻气味,没有刺激性气味。
b.取少量粉末于烧杯中,加足量水,充分搅拌,静置,有固体剩余。
c.取步骤b所得上层清液于试管中,滴入几滴酚酞溶液,溶液不变色。
d.取步骤b所得上层清液于试管中,滴入BaCl2溶液,无明显现象。
【已知:NH4Cl、(NH4)2SO4受热易分解。】
实验操作 | 预期现象与结论 |
若,则粉末的具体成分是。 若,则粉末的具体成分是。 |