文物 |
|
|
|
|
选项 | A.西周五祀卫鼎 | B.唐三彩陶罐 | C.东周漆木尊 | D.汉代玉璧 |
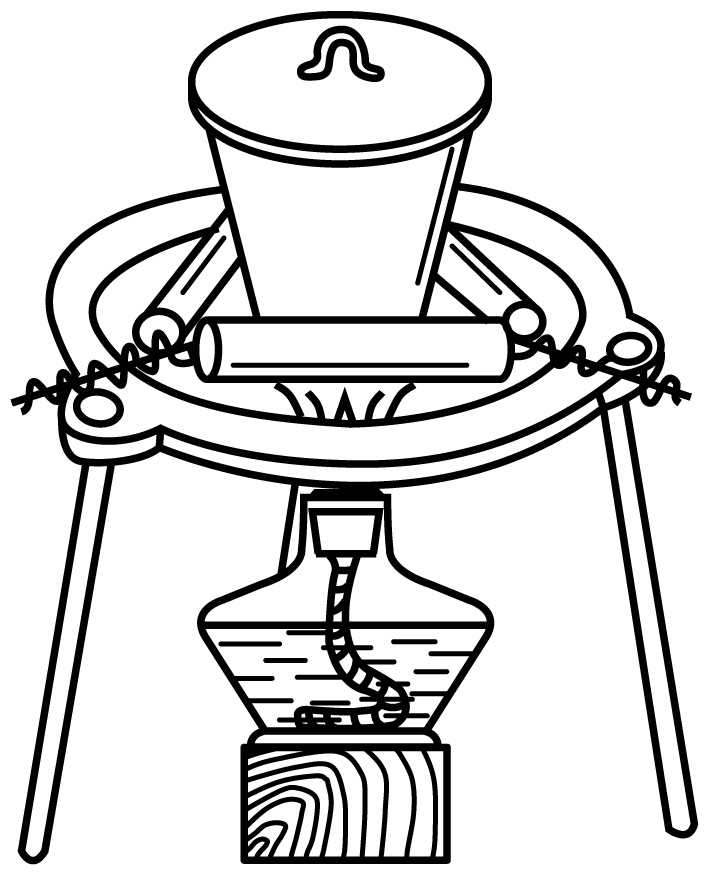 B . 步骤④
B . 步骤④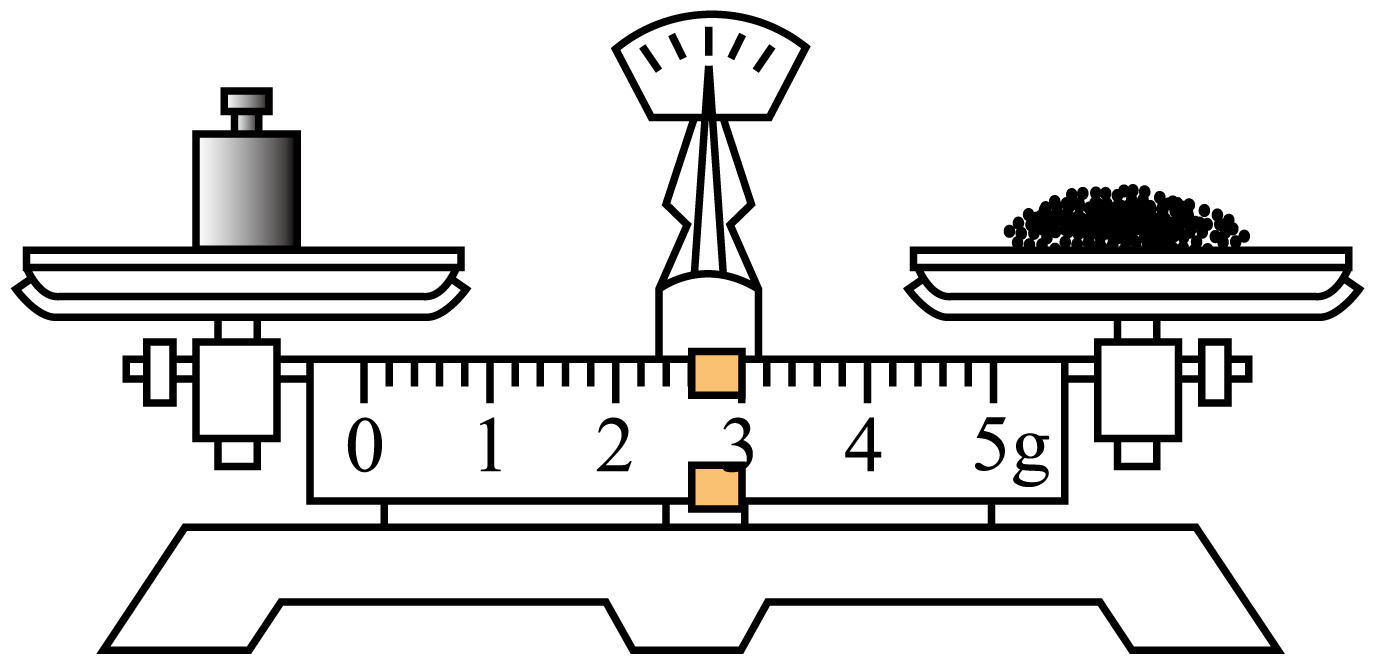 C . 步骤⑤
C . 步骤⑤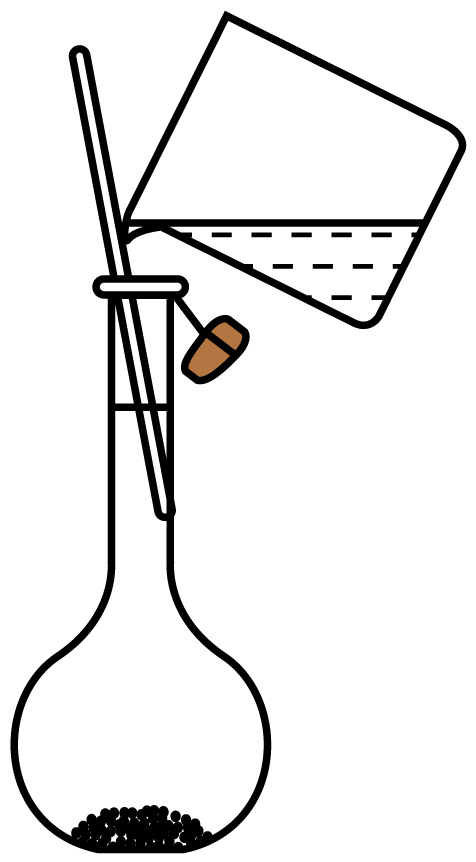 D . 步骤⑥
D . 步骤⑥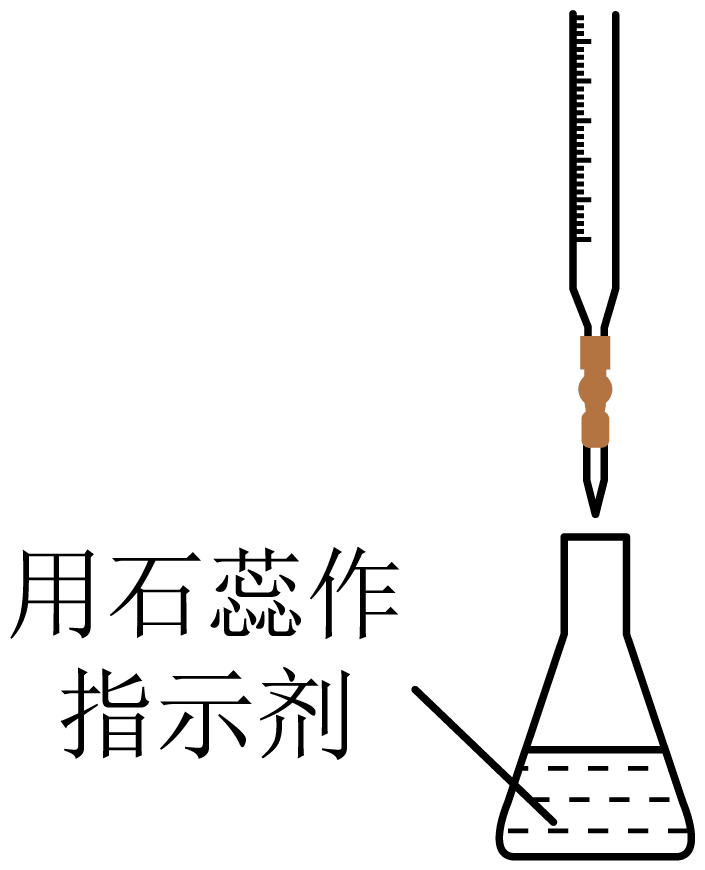

选项 | 劳动项目 | 化学知识 |
A | 传承工艺:使用含淀粉酶的麦芽作用于淀粉,制作饴糖(又称麦芽糖饴) | 麦芽糖水解可生成葡萄糖 |
B | 环保活动:用Fe2(SO4)3作净水剂 | Fe3+水解形成的氢氧化铁胶体可以吸附水中的悬浮物 |
C | 学农活动:向盐碱地(含Na2CO3、NaCl)洒石膏进行处理 | Na2CO3能与CaCl2发生复分解反应 |
D | 学工活动:将铝制品电解氧化形成保护膜 | 铝制品与电源负极相连能够受保护 |


选项 | 陈述I | 陈述Ⅱ |
A | 可用K3[Fe(CN)6]溶液检验铁制品是否发生了吸氧腐蚀 | K3[Fe(CN)6]能与Fe2+反应生成蓝色沉淀 |
B | 相同温度下,0.1mol·L-1NHCl溶液的pH比同浓度NaCl | NH4Cl是弱电解质,NaCl是强电解质 |
C | 向AlCl3溶液中滴加氨水至过量,先产生白色沉淀,之后沉淀溶解 | Al(OH)3是两性氢氧化物 |
D | 非金属性:Cl>Br>I | 沸点:HCl<HBr<HI |
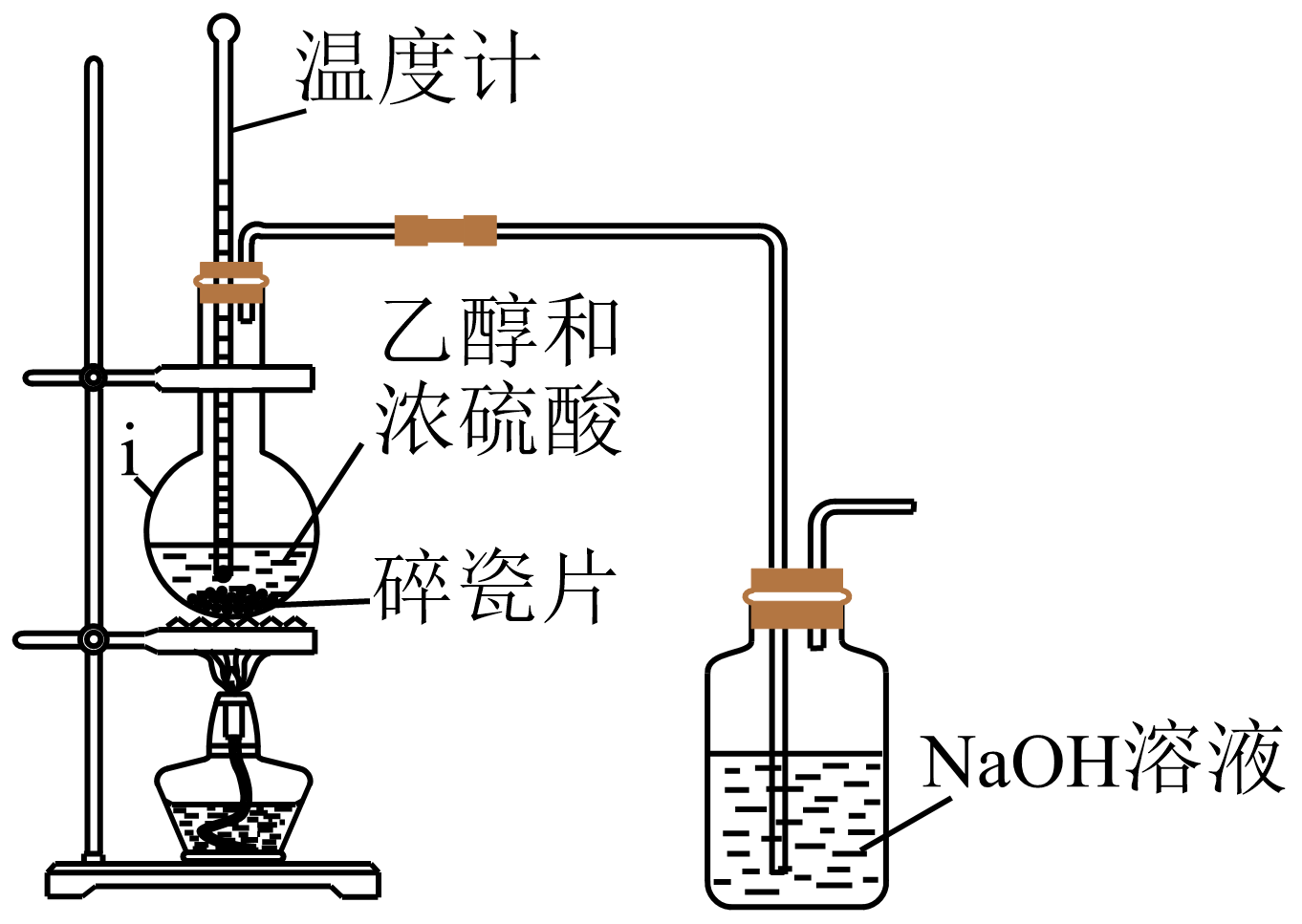
I.制备乙烯
如图所示为制备纯净的乙烯的部分实验装置。
提出猜想1:发生加成反应只生成1,2-二溴乙烷。
验证猜想1
实验操作 | 预期实验现象 | 实际实验现象 |
向一定浓度的溴水中匀速通入足量纯净的乙烯气体,并用pH传感器检测溶液pH的变化。 | ( ),溶液的pH变大 | 溴水褪色,溶液没有明显的分层现象,溶液的pH变小 |
请补充预期实验现象:。预期实验现象中pH变大,请利用平衡移动的原理说明原因:。
提出猜想2:发生取代反应生成1-溴乙烯(实验条件下为不溶于水的无色气体)和HBr。
验证猜想2
实验装置 | 实验操作 | 实验现象 | 实验结论 |
| 1.向装置中加入足量的溴水,同时打开活塞a、b,下压钟罩排尽体系内空气后关闭活塞a; 2.通入适量的乙烯,排出钟罩内部分溴水后,关闭活塞b。静置一段时间 | ( ) | 猜想2不成立 |
说明:通入的乙烯不能过量,要确保溴水未完全褪色。
证明猜想2不成立的实验现象为;通入的乙烯不能过量的原因为。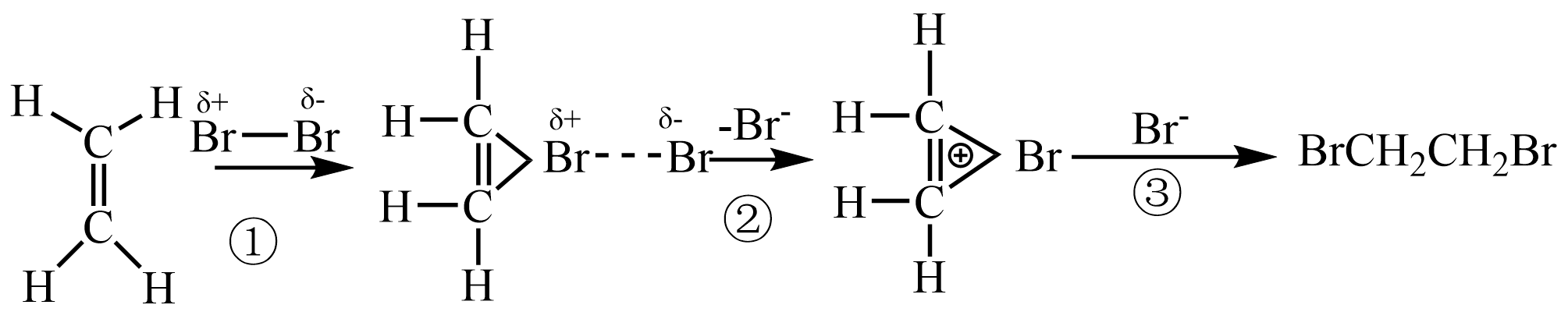
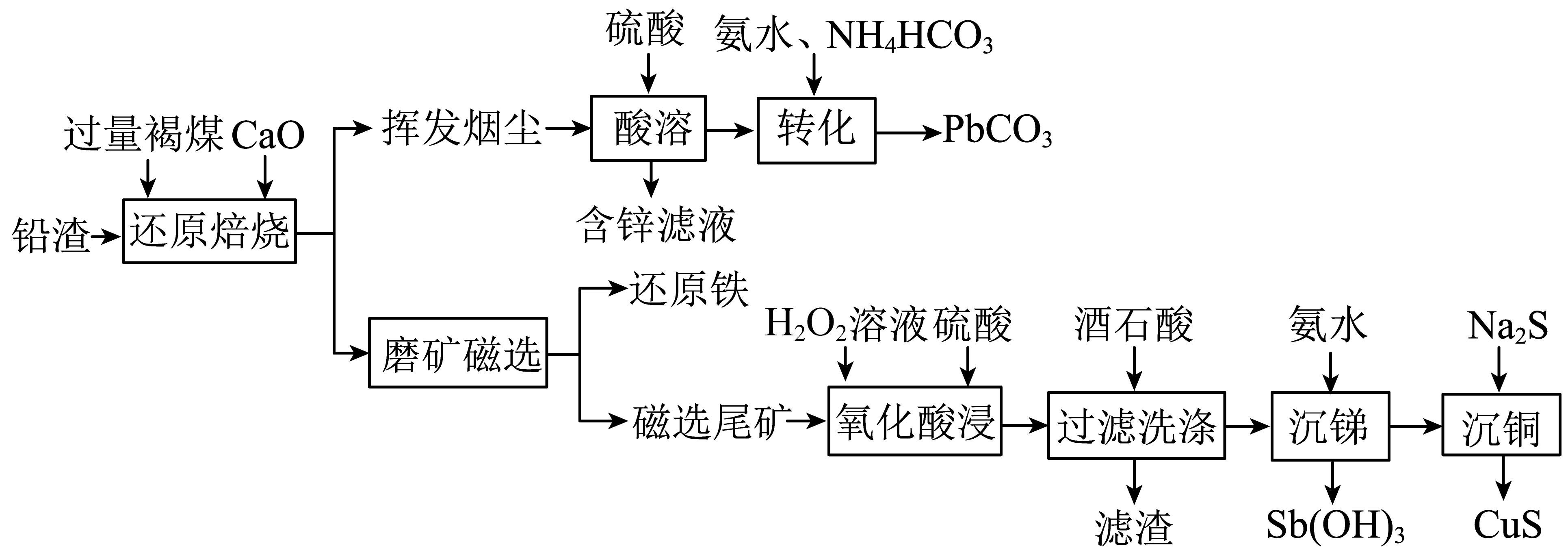
已知:①常温下, ,
金属离子浓度等于时,可认为其恰好完全沉淀。
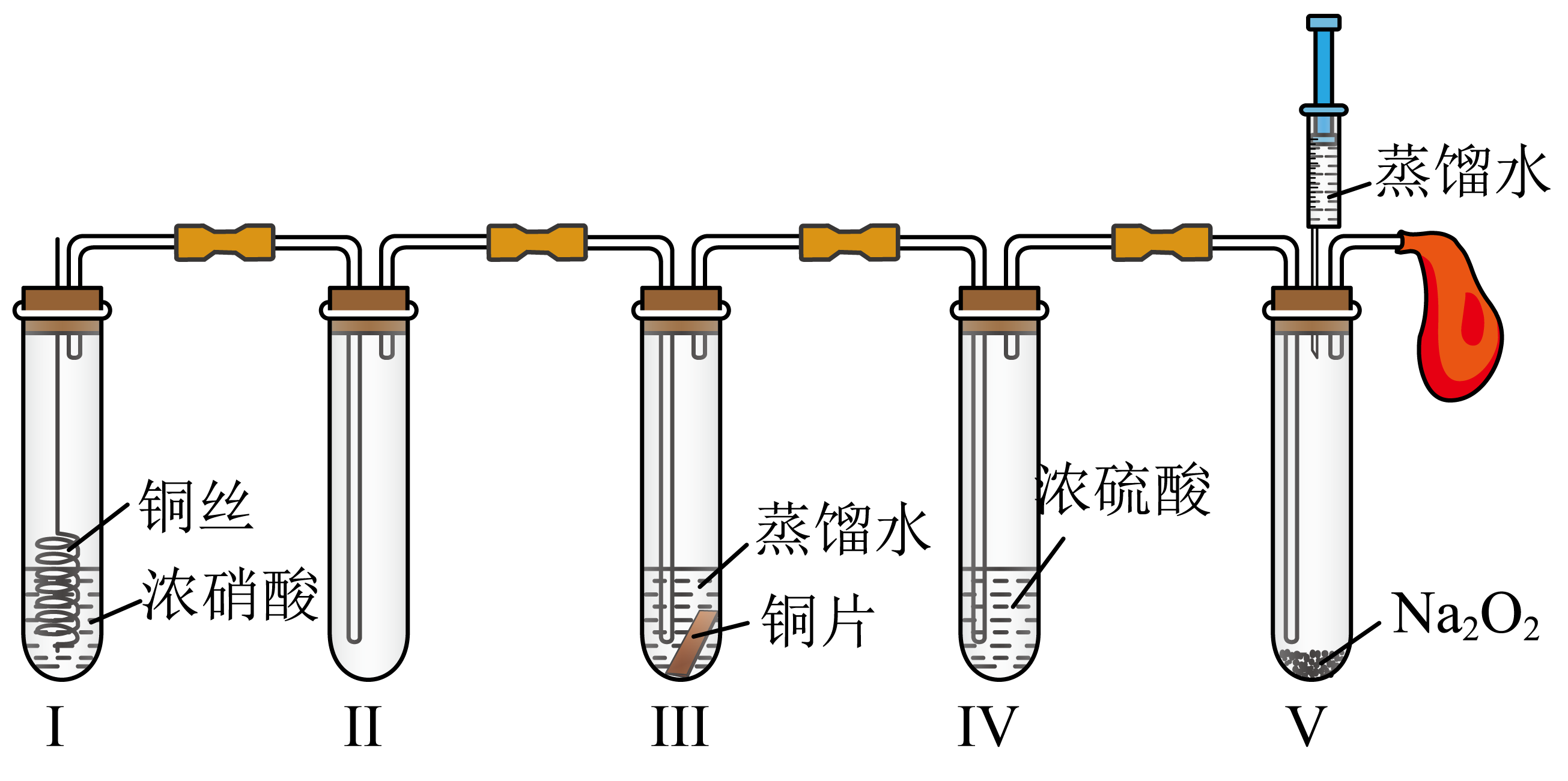
①区分挥发烟尘中的氧化物是晶体还是非晶体的最可靠的科学方法为。
②“转化”过程中,发生反应的化学方程式为。
①上述两个配合物中,提供空轨道的元素为(填元素符号)。
②“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少金属离子的损失,原因为。
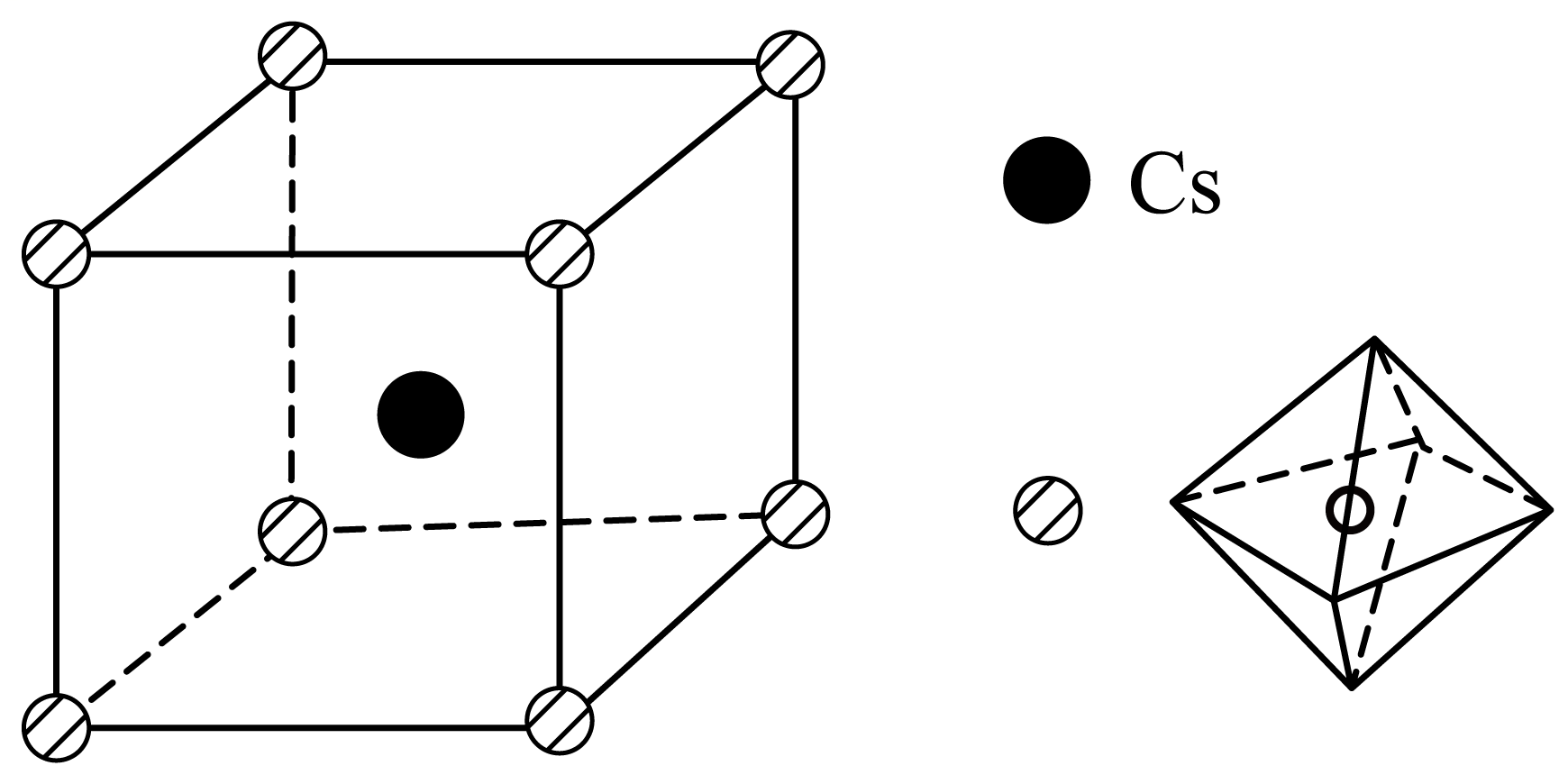
①该晶体的化学式为。
②若该晶体的晶胞以Cs为顶点,则Br在晶胞中的位置为。
++
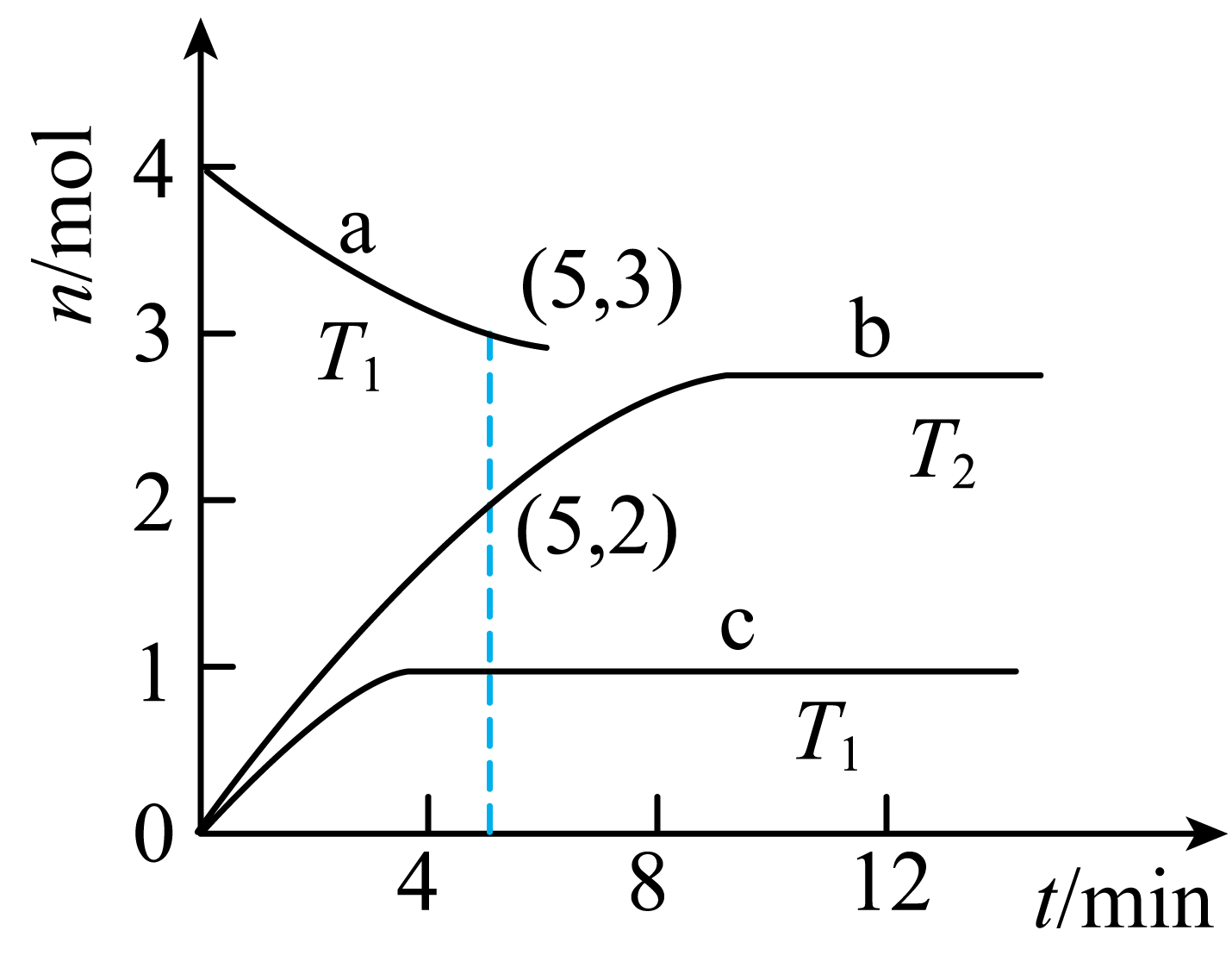
①(填“<”“>”或“=”)。
②在铜-铁催化剂I的作用下,时,
内平均反应速率
。
③上述三种条件下,分解反应的平衡常数的大小关系为
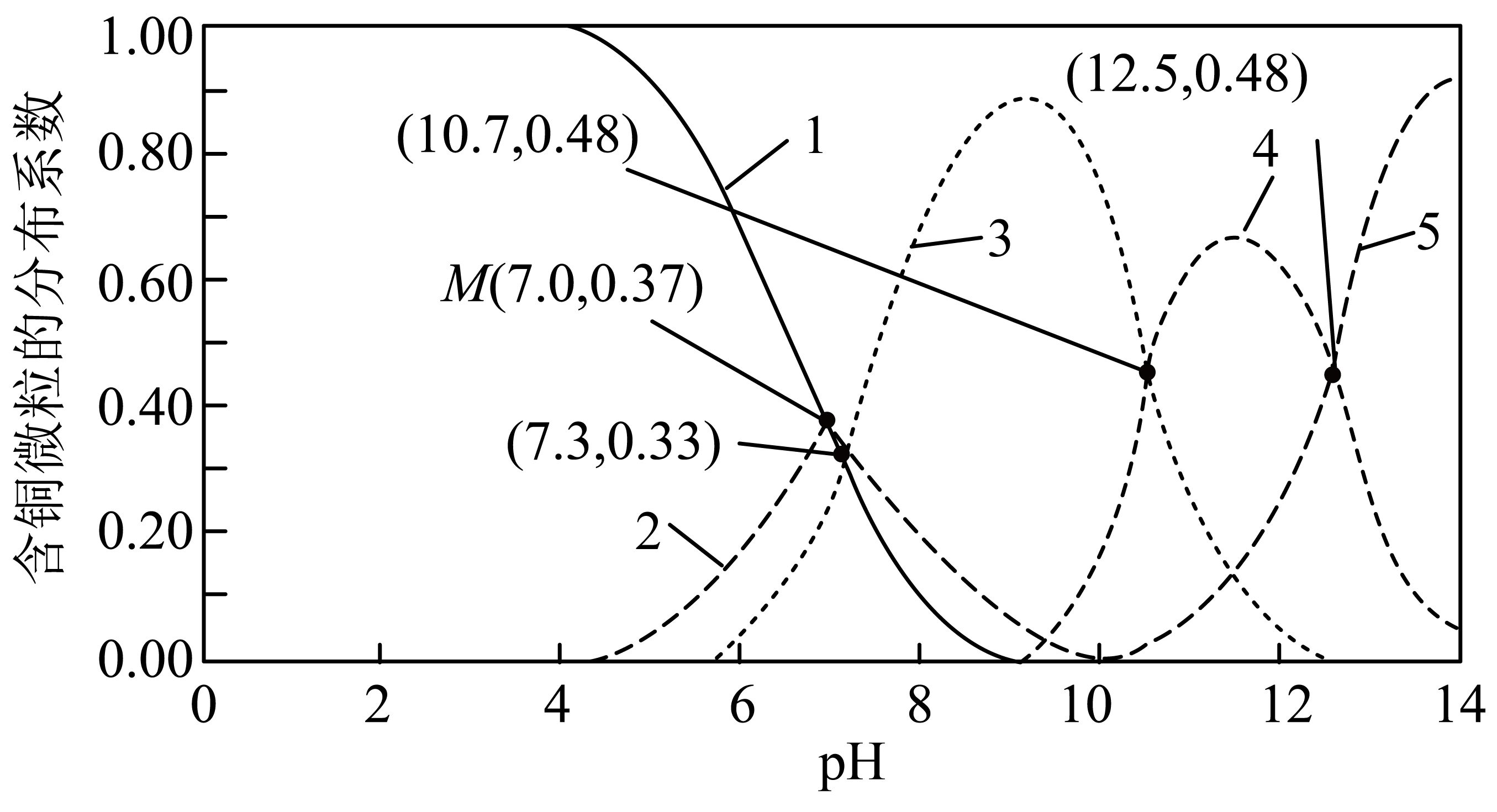
①曲线2代表的含铜微粒为。
②的平衡常数K=。
③若CuSO4溶液起始浓度为 , 加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度(写出计算过程,结果用含
的式子表示)。

序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
a | 加成反应 | ||
b | 取代反应 |
![]() , 其中一种产物v与化合物i反应生成化合物vi。下列说法不正确的有____(填字母)。
, 其中一种产物v与化合物i反应生成化合物vi。下列说法不正确的有____(填字母)。
 。基于你设计的合成路线,回答下列问题:
。基于你设计的合成路线,回答下列问题:(a)反应过程中生成的苯的同系物为(写结构简式)。
(b)相关步骤涉及卤代烃的消去反应,其化学方程式为(注明反应条件)。