 C .
C . 
![]()

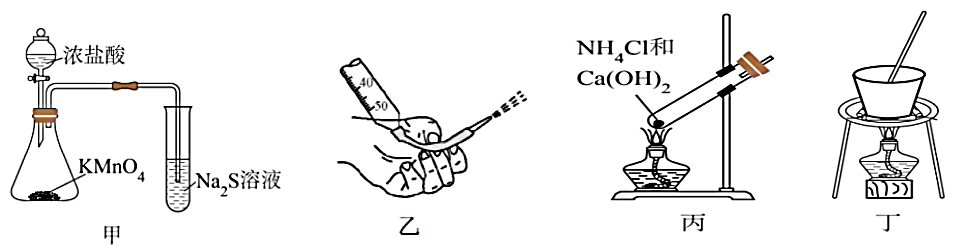
| 目的 | 方案设计 | 现象和结论 |
A | 检验溴乙烷中的溴元素 | 溴乙烷与 | 若有沉淀生成,说明溴乙烷中有溴元素 |
B | 探究 | 室温下,测定 | 若 |
C | 探究钢铁是否发生吸氧腐蚀 | 取钢铁电极附近的溶液,向其中滴加 | 若产生蓝色沉淀,说明钢铁发生吸氧腐蚀 |
D | 探究铁粉与水蒸气反应产物铁的价态 | 取Fe与水蒸气反应后固体,加入足量稀盐酸溶解,再滴加 | 若溶液不变红色,说明产物中没有三价铁 |
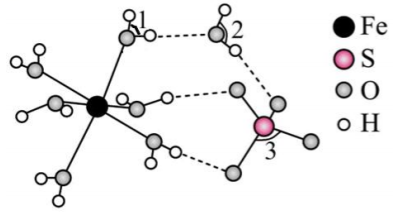 图示
图示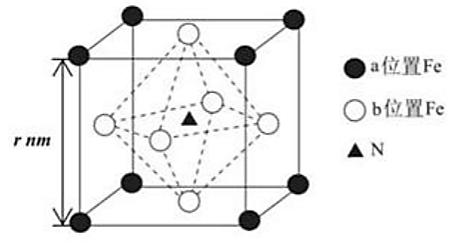
则该反应自发进行的条件是:,。
①该温度条件下反应Ⅰ平衡常数。
②随时间变化数据如下表,一定条件下反应时间t与
的转化关系如下图:

温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
1.00 | 0.70 | 0.50 | 0.20 | 0.20 | ||
1.00 | 0.60 | 0.36 | … | 0.30 |
依据上表数据分析,请在时间t与的转化关系图中标示
,
(假设
)条件下的变化曲线(要求有必要标注)

已知:
回答下列问题:
准确称取样品,用容量瓶配成
溶液;取
上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置
;用
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗
溶液
。
①该样品的有效氯测定值为%。
该样品的有效氯=×100%)
②下列操作会导致样品的有效氯测定值偏高的是(填字母)。
A.滴定管在滴定前仰视,滴定后俯视
B.盛装标准溶液的滴定管未润洗
C.滴定管在滴定前无气泡,滴定后有气泡
D.碘量瓶中加过量的稀硫酸
 )可用于生产治疗血栓栓塞性静脉炎的药物,工业上合成它的一种路线图如下,图中A是苯最简单的一种同系物,G到H的另一生成物是
)可用于生产治疗血栓栓塞性静脉炎的药物,工业上合成它的一种路线图如下,图中A是苯最简单的一种同系物,G到H的另一生成物是
已知:(R、
可以是烃基也可以是氢原子)
请回答:
①遇溶液显紫色
②谱表明:分子中共有4种不同化学环境的氢原子
 开环得到,设计以乙烯为原料合成化合物
开环得到,设计以乙烯为原料合成化合物 的路线(用流程图表示,无机试剂任选)。
的路线(用流程图表示,无机试剂任选)。