
 B . 稀释浓硫酸
B . 稀释浓硫酸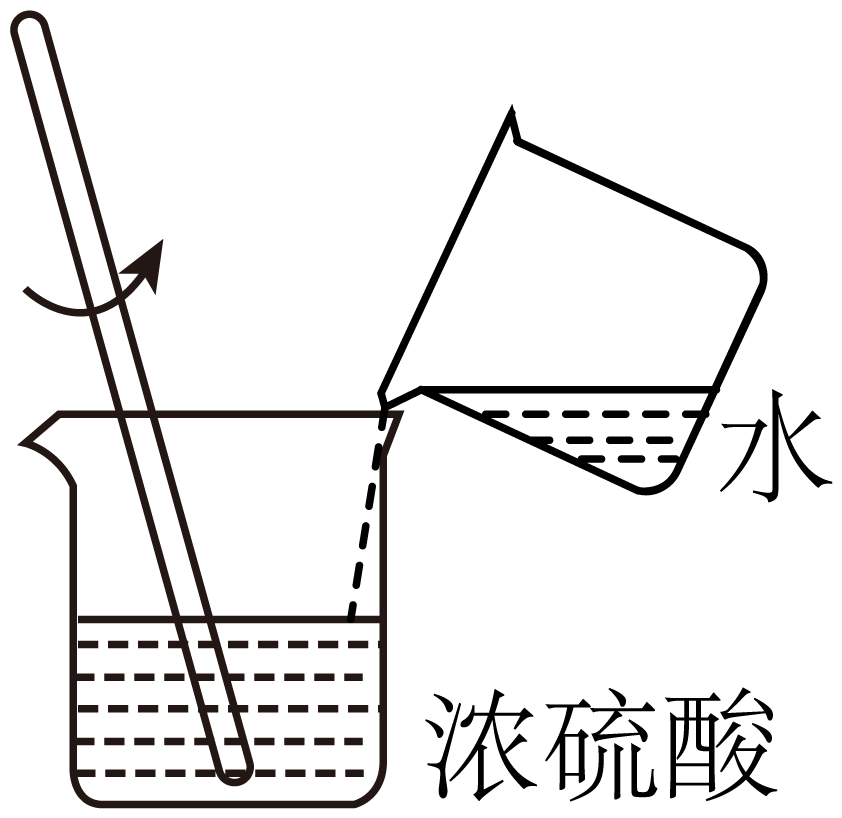 C . 制取氢气
C . 制取氢气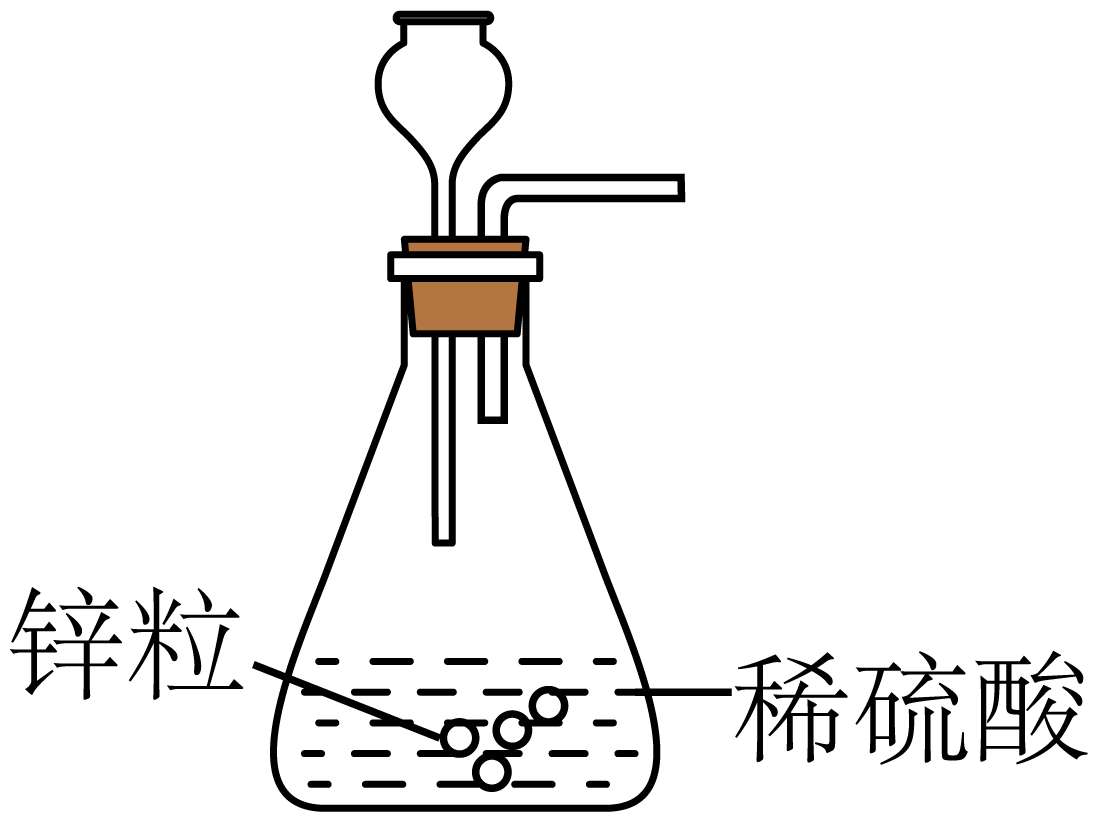 D . 干燥氢气
D . 干燥氢气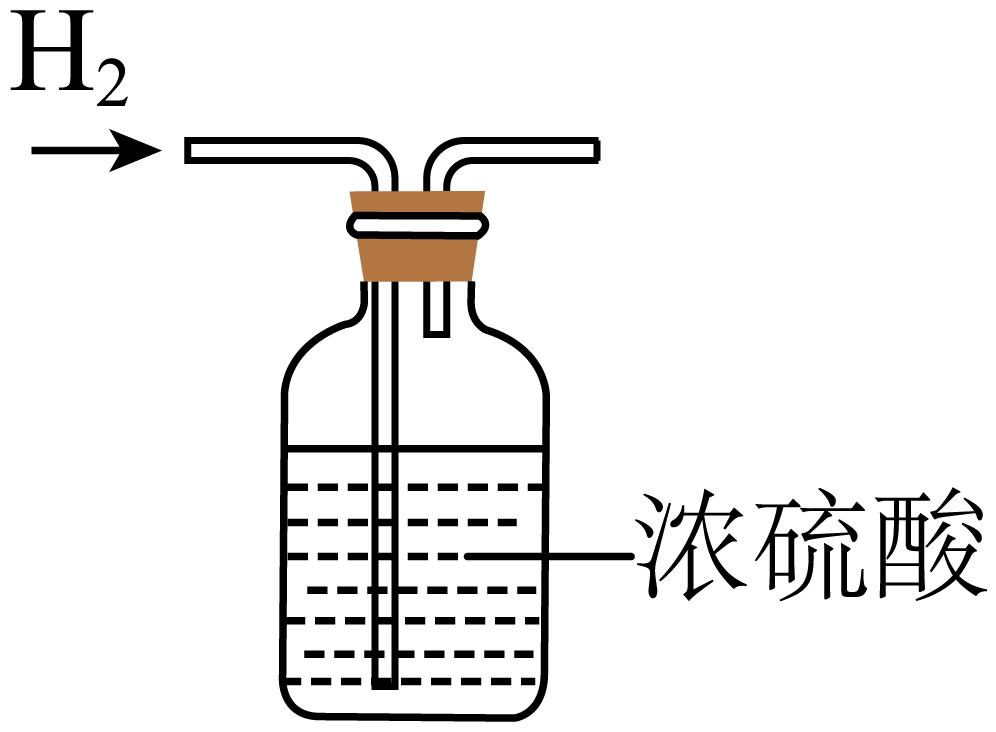
选项 | 劳动项目 | 化学知识 |
A | 向游泳池中撒明矾 | 吸附水中的颜色和异味 |
B | 架空木材生火做饭 | 增加空气中氧气的含量 |
C | 用洗洁精清洗餐具 | 洗洁精可以乳化油脂 |
D | 用稀盐酸除去铁锈 | 酸能与铁锈发生中和反应 |

选项 | 实验目的 | 实验设计 |
A | 区别软水和硬水 | 加入等量肥皂水振荡 |
B | 除一氧化碳中少量二氧化碳 | 将混合气体通过氢氧化钠溶液 |
C | 比较银和铁的金属活动性顺序 | 将打磨后的铁片放入硝酸银溶液中 |
D | 验证质量守恒定律 | 在密闭容器中将铜与稀硫酸混合,比较混合前后物质的总质量 |

2023年9月23日晚,在万众瞩目之下,杭州亚运会的“数字火炬手”与最后一棒火炬手齐心协力点燃了象征亚洲大团结的亚运主火炬。这座主火炬塔历史性地采用了废碳再生的“绿色甲醇”作为燃料,实现了零排放的循环使用。甲醇(CH3OH)俗称“木精”或“木醇”,自身碳含量很低,可以通过二氧化碳加氢生成,每生产1吨绿色甲醇可以消耗1.375吨二氧化碳,实现了二氧化碳的减排和再生利用。所以本届亚运会的火炬被称为“零碳”火炬,准确地说,甲醇火炬是“零增碳”。研究人员使用两种催化剂,探究了影响制备甲醇反应效果的因素。反应效果可用甲醇的选择性衡量,数值越大反应效果越好,结果如下图。研发团队还深入探讨了主火炬燃料使用“零碳”甲醇的可行性。一年内完成理论到实践:两轮专家论证、三轮模拟点火,克服了焰色反应的配比、防风防雨、一次点燃三大挑战,在各种极端条件下成功点火,最终确认执行了方案。

a.3D“数字人”技术 b.直喷火稳焰技术
c.双射流混合防风技术 d.大孔导流防雨技术

a.节约药品 b.方便及时排出废液
c.可以控制反应速率 d.可以控制反应的发生和停止

主要成分 生石灰、苛性钠、铁粉、铝粉、碳粉、氯化钠等 |
任务一:验证发热包中的部分物质
【实验验证】
实验步骤 | 实验现象 | 实验结论 |
Ⅰ、取少许发热包中固体粉末用磁铁靠近 | 有黑色粉末被吸引 | 发热包中含有 |
Ⅱ、向Ⅰ所得剩余固体中加入足量水溶解并过滤,向滤液中滴入酚酞 | 发热包中含有苛性钠 |
经过讨论分析,同学们认为步骤Ⅱ中的实验结论不合理,理由是(用化学反应方程式说明)
任务二:探究发热包的发热原理

为进一步探究发热包中的铁粉能快速发热的原因,同学们按照下表利用图2装置进行实验,得到曲线如图3所示。
实验方案 | 实验药品 |
甲 | 5g铁粉、4mL水、3g氯化钠 |
乙 | 5g铁粉、4mL水、 |
丙 | 5g铁粉、4mL水、3g活性炭、3g氯化钠 |

方案乙需要补充的药品是。
任务三:探究发热包的保存及使用注意事项
久置在空气中的发热包,其主要成分生石灰最终转化成(填化学式),故应密封防潮保存。
