 B . 倾倒液体
B . 倾倒液体 C . 测定溶液pH
C . 测定溶液pH D . 取药液时挤入空气
D . 取药液时挤入空气
 B . 晒干艾叶
B . 晒干艾叶 C . 卷成艾柱
C . 卷成艾柱 D . 燃烧艾柱
D . 燃烧艾柱
 B .
B .  C .
C .  D .
D . 

 咬东西
B .
咬东西
B .  抬起手臂
C .
抬起手臂
C .  踮起脚尖
D .
踮起脚尖
D .  抬起头
抬起头
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
B | CO2(CO) | 氧气 | 点燃 |
C | KCl(K2CO3) | 适量稀盐酸 | 蒸发结晶 |
D | CuO(Cu) | 适量稀硫酸 | 过滤 |
 向氢氧化钾和氯化钡的溶液中逐滴加入稀硫酸
B .
向氢氧化钾和氯化钡的溶液中逐滴加入稀硫酸
B .  向等质量的碳酸钠粉末(a曲线)和碳酸钙(b曲线)中分别加入过量的等浓度的盐酸
C .
向等质量的碳酸钠粉末(a曲线)和碳酸钙(b曲线)中分别加入过量的等浓度的盐酸
C .  向等质量,等溶质质量分数的盐酸中分别逐滴加入镁粉和铝粉
D .
向等质量,等溶质质量分数的盐酸中分别逐滴加入镁粉和铝粉
D .  向一定质量的硫酸铜和稀硫酸混合溶液中逐滴加入氢氧化钠溶液至过量
向一定质量的硫酸铜和稀硫酸混合溶液中逐滴加入氢氧化钠溶液至过量

![]()



实验一:取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得到无色澄清溶液,往溶液中通入CO2 , 产生白色沉淀。
实验二:取14.0g该粉末于烧杯中,加入蒸馏水完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后,产生28.7g白色沉淀。
请回答下列问题:

【猜想与假设】
猜想一:动力×动力臂=阻力×阻力臂
猜想二:动力×支点到动力作用点的距离=阻力×支点到阻力作用点的距离
【设计实验与进行实验】

改变钩码的数量和钩码的位置重复上述实验两次,记录数据如表。
实验次数 | 动力F1/N | OB间距离/cm | 阻力F2/N | OA间距离/cm | |
小科 | 1 | 1.0 | 5 | 0.5 | 10 |
2 | 1.5 | 10 | 1.0 | 15 | |
3 | 1.0 | 10 | 2.0 | 5 | |
小金和小科 | 4 | 0.8 | 15 | 1.0 | 10 |
5 | 1.4 | 15 | 1.0 | 10 | |
【分析与论证】
①根据小科同学的数据可验证猜想 (选填“一”、“二”或“一和二”)是正确的。而小金同学则认为小科同学每组数据中的力臂恰好都等于支点到力的作用点的距离,具有一定的特殊性,还应改变动力或阻力的方向进行实验;
②于是,小金同学协助小科同学按图丙方式进行实验,获得表中后两组数据。综合分析表中数据可验证猜想是错误的;
③通过以上探究,小明同学真正理解了力臂是支点到的距离。

小科进行了猜想:
猜想1:可能是氯化铁溶液变质了。
猜想2:可能是久置的氢氧化钙溶液完全变质了。
针对猜想1,同学们认为猜想不合理,理由是:。
针对猜想2,小科取少量氢氧化钙溶液,向其中加入酚酞溶液,出现,说明氢氧化钙溶液没有完全变质
小科查阅资料发现:氯化铁溶液呈弱酸性,氢氧化钠易溶于水,氢氧化钙微溶于水。
同学们在原实验器材的基础上,调整了方案,在氢氧化钙溶液与氯化铁溶液反应的实验中也看到了红褐色絮状沉淀,请写出实验方案:。

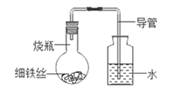
【实验步骤】取一条长为15cm,宽4cm的铁片用砂纸将其打磨干净,水平固定在铁架台上,然后将研细的硫粉和铁粉混合均匀后,在铁片上铺成细条状,然后用酒精灯在铁片的一端加热,待部分药品红热后停止加热。
【实验现象】观察到铁片上残留有黑色固体,并闻到一股刺激性气味。
【进行实验】小科同学取少量溶液于试管中,滴入几滴无色酚酞,观察到溶液变红,小科同学认为溶液中一定有NaOH。
【交流与评价】小金同学认为小科同学的结论不一定正确,原因是。于是,小组同学继续进行探究。
实验操作 | 实验现象 | 实验结论 |
小金同学在小科同学所做实验后的溶液中,滴入过量的Ba(NO3)2溶液 |
| 一定没有NaOH |
小组同学继续探究,最终证明该Na2CO3溶液只含有Na2SO4一种杂质,请在小金实验的基础上补充实验步骤并描述实验现象。
另取少量该Na2CO3溶液进行以下实验,也能证明溶液中NaOH不存在的是____(填序号)。
Ⅰ.查阅资料:①Cu2O属于金属氧化物; ②高温灼烧CuO生成Cu2O;
③Cu2O+H2SO4=Cu+CuSO4+H2O;④3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
⑤3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O 。
Ⅱ.设计实验方案:方案1:取该红色试样溶于足量的稀硝酸中,观察溶液是否呈蓝色;
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色。

为确保探究的科学、合理、安全,你认为实验中还应采取的措施有:____(填序号)。


名称 | Ca(OH)2 | NaOH |
价格(元/kg) | 6.00 | 24.00 |
实验编号 | 第一次 | 第二次 | 第三次 | 第四次 |
加入氢氧化钠溶液质量/g | 10 | 10 | 10 | 10 |
烧杯中生成沉淀的总质量/g | 0.29 | 0.87 | 1.45 | 1.45 |
请计算:


①在实际生产中,经常用NaOH溶液来“捕捉”CO2 , 流程如图丁所示(部分条件及物质未标出)。用该技术进行“碳捕获”有效利用了原材料,该过程中被循环利用的物质有。
②每生产100吨甲醇,可直接减排二氧化碳吨,实现了二氧化碳的资源化利用。
