
| 选项 | 物质 | 杂质(少量) | 操作方法 |
| A | N2 | O2 | 将混合气体通过灼热的碳粉 |
| B | NaOH溶液 | Na2CO3溶液 | 加入适量氢氧化钙溶液,过滤 |
| C | 氯化钠固体 | 泥沙 | 加水溶解,蒸发结晶 |
| D | KCl溶液 | K2SO4溶液 | 加入适量Ba(NO3)2溶液,过滤 |
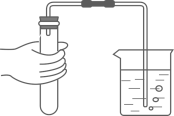 B . 稀释浓硫酸
B . 稀释浓硫酸 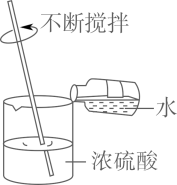 C . 滴管取液
C . 滴管取液 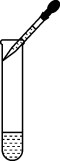 D . 测定某溶液的pH
D . 测定某溶液的pH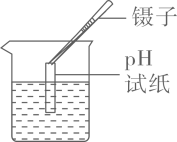


试剂 | 稀盐酸 | 氢氧化钠溶液 | 蒸馏水 | 白醋 | 氨水 |
滴加2滴紫薯汁后显示的颜色 | 红色 | 绿色 | 紫色 | 红色 | 绿色 |
混合物 单质 氧化物 盐


①硝酸钙与碳酸铵在溶液中反应 ,其基本反应类型为。
②高纯氧化钙生产过程中 ,“干燥”的主要目的是防止(用化学方程式表示)。


为了鉴别它们:先把两支试管分别贴上标签①、②,然后进行如下实验。
实验步骤 | 实验现象 | 结论 |
各取少量未知无色溶液于①②两支试管中,分别滴加碳酸钠溶液 | ①中无明显现象 ②中产生白色沉淀 | ①试管中加入的无色溶液为____ |
【提出问题】反应后溶液中溶质的成分是什么?
【作出猜想】猜想一:氢氧化钠 猜想二: 猜想三:氢氧化钠和碳酸钠
【验证猜想】若通过下列实验得出猜想三成立,请写出相应的实验过程与现象。
实验过程 | 实验现象 | 实验结论 |
猜想三成立 |
【发现问题】 氯水中的哪种成分能使品红褪色呢?
【查阅资料】 氯气溶于水,部分与水反应,方程式为Cl2+H2O=HCl+HClO。 其中 HClO 的名称叫次氯酸,是一种弱酸 ,具有强氧化性。
【猜想】
猜想1:……
猜想2:是氯水中的“氯气”使品红褪的;
猜想3: 是氯水中的“HCl”使品红褪的;
猜想4: ……
【实验探究】
实验操作 | 实验现象 | 过程分析 |
①把品红试纸伸入水中 | 没有褪色 | 猜想 1 不成立 |
②把品红试纸伸入干燥的氯气中 | 没有褪色 | 猜想 2 不成立 |
③把品红试纸伸入____ 中 | 没有褪色 | 猜想 3 不成立 |
【结论】综合以上实验可以猜想 4 成立 ,得出的结论是:。

实验前,先通了一段时间的N2 , 点燃丙处酒精灯,发现丙处固体未变色。然后再点燃甲处酒精灯。反应开始后甲中固体变红,若观察到现象,说明反应产生了 CO和CO2。
小组成员取了5份等质量的CuO,在不同温度下与C 反应,4小时后测得固体物质的XRD 图谱图像。为确保反应后的固体产物不含 Cu2O,据图分析可以采取怎样的措施?。


如下是该项目成员对微型实验设计的评价量表,请你帮助小组成员再添加一个评价维度,并写出一条待改进的原因。
评价维度 | 优秀 | 待改进 |
可行性 | 实验原理科学 | 实验原理有误 |
操作性 | 操作简便 | 操作复杂 |
经济性 | 药品用量节省 | 药品用量较多 |
__ | …… |

实验次数 | 一 | 二 | 三 | 四 | 五 | 六 |
稀硫酸的用量/g | 20 | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 7.0 | M | 4.2 | 2.8 | 1.4 | 1.4 |