
选项 | 意外事故 | 处理方法 |
A | 洒在桌面上的酒精燃烧起来 | 立即用湿抹布或沙子扑灭 |
B | 水银不小心洒在地上 | 可先用硫粉盖住过会再清理 |
C | 浓硫酸溅到皮肤上 | 立即用大量水冲洗 |
D | 碱液泼在皮肤上 | 用水冲洗后,再涂上硼酸溶液 |
选项 | 物质 | 杂质 | 除杂试剂及操作方法 |
A | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
B | 氢气 | 氯化氢 | 先通过过量氢氧化钠溶液,再通过过量浓硫酸 |
C | 锌粉 | 铁粉 | 加入适量氯化锌溶液,充分反应后过滤 |
D | 氯化钾溶液 | 碳酸钾 | 加入过量氯化钙溶液,充分反应后过滤 |
乙同学计算出合金中铜的质量分数为: .
经过同学们讨论,一致认为同学的计算结果是错误的,原因是.

证明 | 实验方案 |
酸性 | 方案一:取少量稀释液,加入金属锌 |
方案二:取少量稀释液,加入氢氧化钠溶液 | |
方案三:取少量稀释液,加入碳酸钠溶液 |
①小明设计的实验方案可行的是;
②下列对生活污水的处理,你认为合理的是(选填序号).
A.洗脸水、厨房用水等可以用来冲洗马桶
B.用“洁厕灵”清洗洁具后的冲刷液不能用来直接灌溉农田
C.全面规划,合理布局,进行区域性综合治理.

操作一:分别取真假珍珠粉各少许置于两只试管中,加一定量的稀盐酸后迅速塞紧橡皮塞,将导管的另一端放入石灰水中,观察发现:试管a中均有气泡产生;试管b中实验现象为:由此可得结论:都含有碳酸盐;
操作二:分别取真假珍珠粉少许置于铁片上灼烧,发现前者能闻到烧焦羽毛气味;后者未闻到烧焦羽毛气味,由此可得出结论:假珍珠粉中不含.
【提出问题2】真假珍珠粉中碳酸钙的含量有差别吗?
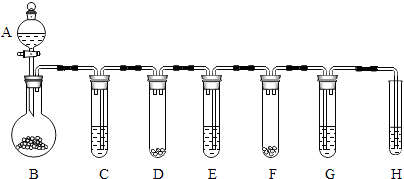
【实验2】各取5g真假珍珠粉各稍许,置于下列实验装置中(稀盐酸足量).测定生成气体体积数据如下:
样品种类 | 第一次 | 第二次 | 第三次 |
假珍珠粉样品(mL) | 110.50 | 110.28 | 110.05 |
真珍珠粉样品(mL) | 103.82 | 103.16 | 102.82 |
回答相关问题:
①量气管点上端加一层植物油的目的是.
②由实验数据可知:真珍珠粉中碳酸钙的含量假珍珠粉(填“>”、“<”、“=”).

方案二:样品 测定剩余固体质量.
具体操作步骤如下:
①一只洁净的坩埚,称得质量为21.2克,再向其中加入样品,称得总质量为41.2克;
②加热盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为35.0克.
(已知2NaHCO3 Na2CO3+H2O+CO2↑)