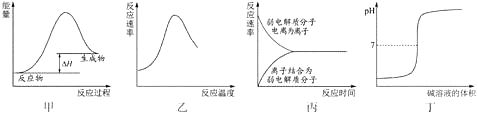



步骤1:按图所示组装仪器,检查装置气密性。
步骤2:在相应仪器中装入药品,其中在三颈烧瓶中加入氢氧化钠固体,恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品
……
①干燥管中盛放的药品是。
②对比碳酸盐和酸反应制CO2 , 该实验利用干冰升华产生CO2气体的优点有,。
③以恒压滴液漏斗代替分液漏斗的目的是。
④反应后期CO2气流量下降时,可采取的相应措施是。

注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
化学式 | 沉淀完全时的pH | 钴镍性质 |
Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
Fe(OH)2 | 9.6 | |
Fe (OH)3 | 3.7 |
加NH3·H2O调pH | 收率/% | Ni2+含量/% |
9 | 98.1 | 0.08 |
9.5 | 98 | 0.05 |
10 | 97.6 | 0.005 |
10.3 | 94 | 0.005 |
②2CO(g)+O2(g)=2CO2(g) ΔH=-1200 kJ•mol-1 。
则5CO(g)+I2O5(s)=5CO2(g)+I2(s)的△H= 。
① I2(s)+I-(aq) I3-(aq) △H<0; ② I2 (s)+2I-(aq)
I42-(aq)。
温度降低时,反应①的平衡常数将(填“增大”“减小”或“不变”);反应②的平衡常数的表达式为K=。

① 该反应△H0(填“>”或“<”)。
② 反应从开始到t1(t1= 3 min)时间内 I2 的平均反应速率v(I2)=。
③ 在450℃时,该反应的平衡常数K的值为。
④ 能够说明上述反应已经达到平衡状态的有 (填选项字母)。
A.I2与WI2的浓度相等
B. 容器内各气体的浓度不再改变
C. 容器内混合气体的密度不再改变
D.容器内气体压强不发生变化
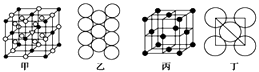
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为个; Al晶体的密度为(用字母表示)。

① 属于芳香族化合物; ② 苯环上的一取代物只有两种;
③ 在铜催化下与O2反应,其生成物1 mol与足量的银氨溶液反应生成4 mol Ag
ROH+SOCl2![]() RCl+HOSOCl
RCl+HOSOCl
请写出合成卡巴拉丁流程中A、B、D的结构简式,C试剂的化学式。

A:、B:、C:、D:。