


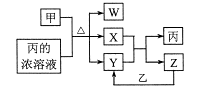

已知: CS2和H2S均有毒:CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
①仪器d的名称是。反应开始时需要先通入一段时间N2 , 其作用为。
②B中发生反应的离子方程式是。
③反应结束后打开活塞k,再缓慢通入热N2 一段时间,其目的是。
④为了计算三硫代碳酸铀溶液的浓度,可测定B中生成沉淀的质量。称量B中沉淀质量之前需要进行的实验操作名称是,若B中生成沉淀的质量为8.4g则35.0 mL三硫代碳酸钠溶液的物质的量浓度是。
⑤若反应结束后将通热N2改为通热空气,通过测定C中溶液质量的增加值来计算三硫代碳酸钠溶液的浓度时,计算值<填“偏高”“偏低”或“无影响”)。

按元素周期表的对角线规则,Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如表。回答下列问题:

A. 3.3-3.7 B. 3.7—5.0 C. 5.0~5.2 D.5.2—6.5
S(s)+ O2(g)=SO2(g) △H2
2S(s) S2(g) △H3
2H2S(g)+SO2(g)=3S(s)+2H2O(g) △H4
则反应2H2S(g) 2H2(g)+ S2(g)的△H=
在恒容密闭容器中,阻H2S的起始浓度均为0.009 mol/L控制不同温度进行H2S分解:2H2S(g) 2H2(g)+ S2(g) ,实验过程中测得H2S的转化率如图所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度F反应经过相同时间时H2S的转化率。

①在935℃时,该反应经过t s H2S的转化率达到P点数值,则在ts内用H2浓度变化表示的平均反应速率v(H2)=。
②温度升高,平衡向方向移动(填“正反应”“逆反应”),平衡常数(填“增大”“减小”或“不变”)。985℃时该反应的平衡常数为。
③随着H2S分解温度的升高,曲线b逐渐向曲线a靠近,其原因是。

①进入电解池的溶液中,溶质是。
②阳极的电极反应式为。
③电解总反应的离子方程式是。
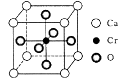
翡翠是玉石中的一种,其主要成分为硅酸铝钠-NaAI(Si2O6),常含微量Cr、Ni、Mn、Mg、Fe等元素。回答下列问题:
若其中有一半的Si被Al替换,其化学式为。
a.0.1 molM与足量金属钠反应生成氢气2.24 L(标准状况)
b.同一个碳原子上不能连接2个羟基
其中核磁共振氢谱显示3组峰,且峰面积之比为3:1:1的结构简式是。