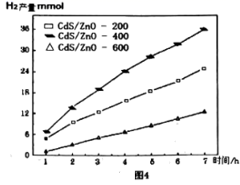
I.热分解制氢:H2S在高温下分解生成硫蒸气和H2。
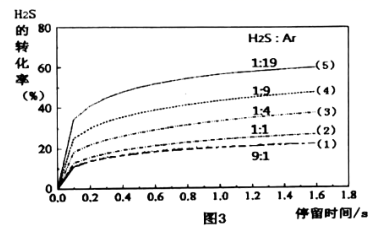
①101kPa时,改变H2S与Ar物质的量之比1:19充入容器甲。保持压强不变,反应在不同温度下达到平衡时,反应物和生成物的气体体积分数如图1和图2所示;
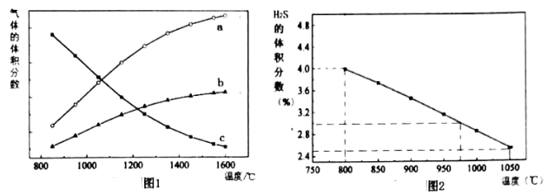
②1100℃,101kPa时,改变H2S与Ar的物质的量之比,将气体充入容器乙。保持压强不变,H2S的转化率随停留时间变化如图3;
③Kp:对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp。如p(B)=p•x(B),P为平衡总压强,x(B)为平衡系统中B的物质的量分数:
④停留时间:停留时间也称接触时间,指原料在反应区或在催化剂层的停留时间。
A.b曲线对应物质的分子式为S2
B.随温度升高,容器甲内气体密度减小
C.H2S热分解的活化能大于其逆反应的活化能
D.由图3可知H2S的浓度越低,热分解反应的速率越大