 D .
D . 
| 时间/s | 0 | 2 | 10 | 30 | 60 | 90 |
| n(N2O4)/mol | 0.3 | 0.25 | 0.15 | 0.125 | b | 0.12 |
| n(NO2)/mol | 0 | 0.1 | a | 0.35 | 0.36 | 0.36 |
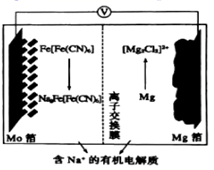
下列说法正确的是( )
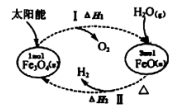
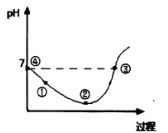
下列叙述中正确的是( )
|
实验序号 |
铁片单侧面积/cm2 |
反应前质量/g |
反应后质量/g |
|
1 |
25.05 |
14.625 |
13.803 |
|
2 |
24.95 |
14.566 |
13.746 |
|
3 |
24.89 |
14.489 |
12.789 |
该镀锌铁皮锌镀层厚度为cm(保留2位有效数字);写出简要计算过程。
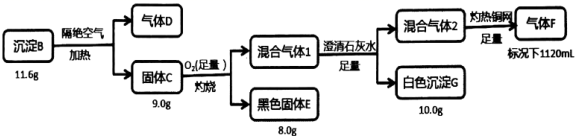
已知:B含三种元素;气体D标况下密度2.32g/L;混合气体l无色无味;气体F标况下密度为1.25g/L。请回答:
①X分子结构中不含碳碳双键和羟基②X核磁共振氢谱有三组峰
请回答:
I.热分解制氢:H2S在高温下分解生成硫蒸气和H2。
①101kPa时,改变H2S与Ar物质的量之比1:19充入容器甲。保持压强不变,反应在不同温度下达到平衡时,反应物和生成物的气体体积分数如图1和图2所示;
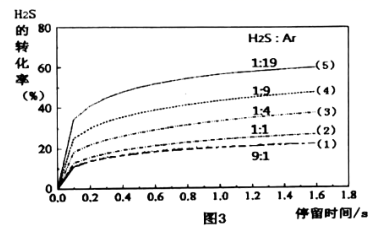
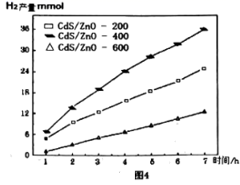
②1100℃,101kPa时,改变H2S与Ar的物质的量之比,将气体充入容器乙。保持压强不变,H2S的转化率随停留时间变化如图3;
③Kp:对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp。如p(B)=p•x(B),P为平衡总压强,x(B)为平衡系统中B的物质的量分数:
④停留时间:停留时间也称接触时间,指原料在反应区或在催化剂层的停留时间。
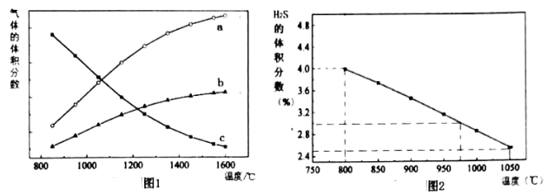
A.b曲线对应物质的分子式为S2
B.随温度升高,容器甲内气体密度减小
C.H2S热分解的活化能大于其逆反应的活化能
D.由图3可知H2S的浓度越低,热分解反应的速率越大
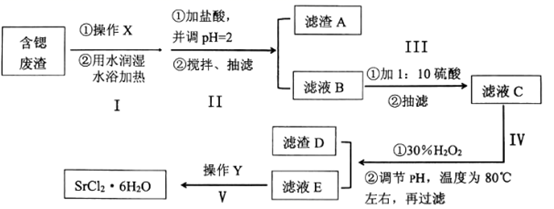
已知:①SrSO4微溶于水;
②SrCl2•6H2O在61.5℃以上即会失去4个结晶水生成SrCl2•2H2O。
|
硫酸加入量/mL |
4.50 |
4.95 |
5.40 |
5.85 |
6.30 |
|
Ba2+/(g/L) |
0.37 |
0.21 |
0.13 |
0.11 |
0.10 |
|
Sr2+/(g/L) |
90.21 |
89.86 |
89.57 |
89.23 |
88.90 |
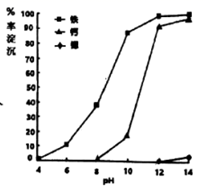
②往滤渣D中加入NaClO溶液,发生反应的离子方程式为:。
滤液E→()→()→()→抽滤→()→()
a.蒸发浓缩至有大量晶体析出
b.在过饱和溶液中加入晶种
c.6l.5℃以上减压蒸发浓缩
d.6l.5℃以下减压蒸发浓缩
e.往溶液中加入无水乙醇
f.在30℃真空烘箱中干燥
g.在室温下缓慢冷却结晶
h.用氯化锶饱和溶液洗涤晶体
I.用冷水洗涤晶体
①判断滴定终点的现象为;
②实验时未采用棕色滴定管滴定,会使测得的晶体纯度(填“偏高”、“偏低”或“不变”)。