|
温度/℃ |
400 |
500 |
|
平衡常数K |
9 |
5.3 |
①该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的△S(填“>”或“<”")0。
②在容积为10 L的密闭容器中通入0.1 mol CO(g)和0.1 mol H2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为。
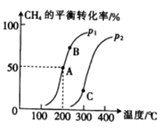
①200 ℃时,该反应的平衡常数K=。
②A、B、C三点的平衡常数KA、KB、KC的大小关系是。
③压强:p1 (填“>”“<”或“=”)p2。
微信扫码预览、分享更方便