
已知①“沉淀”时需控制温度为0℃左右。
②CaO2•8H2O是白色晶体粉末,难溶于水.
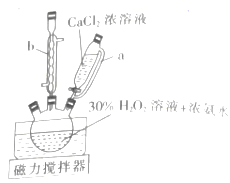
①“沉淀”时控制温度为0℃左右的原因是。
②仪器a的名称是,仪器b的作用是。
第一步:准确称取ag产品于锥形瓶中,加入适量的蒸馏水和bgKI晶体(过量).再滴入适量盐酸溶液充分反应。
第二步:向锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为cmol•L-1的Na2S2O3溶液至滴定终点,消耗Na2S2O3溶液VmL。
已知:2 +I2=2I-+
。
①第二步滴入几滴淀粉溶液时,溶液呈(填“无色”或“蓝色”)。
②产品(CaO2)的纯度为(列出计算表达式)。

①装置A中发生反应的化学方程式为。
②装置B中浓H2SO4的作用是。
③装置E用于测定O2的体积,请在框中画出装置图。