1.
(2021·云南模拟)
镍及其化合物在工业上有广泛应用,红土镍矿是镍资源的主要来源。以某地红土镍矿[主要成分Mg3Si2O5(OH)4、Fe2MgO4、NiO、FeO、Fe2O3]为原料,采用硫酸铵焙烧法选择性提取镍,可减少其他金属杂质浸出,工艺流程如图所示。
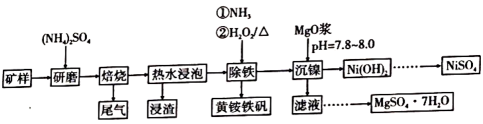
已知:①2[Mg3Si2O5(OH)4]+9(NH4)2SO4 3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
②2Fe2MgO4+15(NH4)2SO4 (NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
(NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
③常温下,NiSO4易溶于水,NiOOH不溶于水。
-
(1)
“焙烧”前将“矿样”与(NH4)2SO4混合研磨的目的是。
-
-
(2)
经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与(NH4)2SO4反应生成Fe2(SO4)3 , 该反应的化学方程式为,“浸渣"的主要成分除铁的氧化物外还有(填化学式)。
-
-
(3)
焙烧温度对浸出率的影响如图所示,最佳焙烧温度是____(填序号)左右。
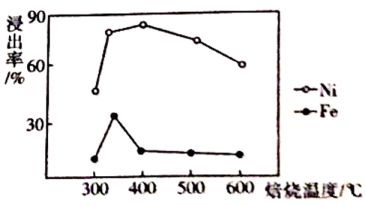
A . 300℃
B . 350℃
C . 400℃
D . 600℃
-
-
(4)
若残留在浸出液中的铁完全转化为黄铵铁矾除去,“除铁”时通入NH
3调节溶液pH的范围是
。该工艺条件下,Ni
2+生成Ni(OH)
2沉淀,Fe
3+生成Fe(OH)
3或黄铵铁矾沉淀定,开始沉淀和沉淀完全时的pH如下表:
沉淀物 | Ni(OH)2 | Fe(OH)3 | 黄铵铁矾 |
开始沉淀时的pH | 7.1 | 2.7 | 1.3 |
沉淀完全(c=1×10-5 mol/L)时的pH | 9.2 | 3.7 | 2.3 |
-
-
(5)
“沉镍"时pH调为8.0,滤液中Ni2+浓度约为mol/L(100.4≈2.5)。
-
-
-
-
(7)
NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式是。
-

3(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
(NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
