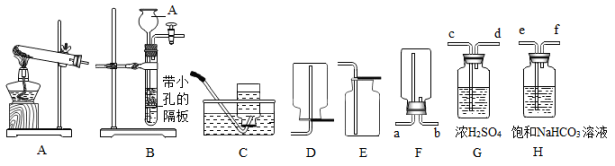
①指出编号仪器名称:A。
②实验室若用加热高锰酸钾固体的方法制取氧气,选择的发生装置是。
③实验室制取并收集二氧化碳应选择的装置是(从A-E中选择),使用该套装置制取气体的突出优点是,改用F装置收集二氧化碳,如何验满。制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→(用端口字母表示)。
【查阅资料】①镁能与水缓慢反应生成氢气。
②Na2CO3、K2CO3溶液均显碱性,其溶液中除金属离子、
外,还有OH-。
实验1:探究反应产生的气体
【猜想与假设】
Ⅰ、气体是H2
Ⅱ、l气体是CO2
Ⅲ、气体是H2和CO2
【进行实验】取适量镁条、100mL饱和Na2CO3溶液,按如图所示方案进行实验。
| 据号 |
1-1 |
1-2 |
| 装置 |
|
|
| 实验现象 |
澄清石灰水 |
气体被点燃,烧杯内壁有小液滴生成 |
【猜想与假设】Na2CO3溶液中的某一种离子促进了镁与水的反应,从而产生较多气体。
【进行实验】20℃时,利用图示装置分别完成下列实验,记录如下:
| 装置 |
编号 |
实验操作 |
实验现象 |
|
|
2-1 |
向试管中加入2mL17.7%的Na2CO3溶液 |
持续产生较多气泡 |
| 2-2 |
向试管中加入2mL1%的Na2CO3溶液 |
有少量气泡 |
|
| 2-3 |
向试管中加入2mL17.7%的K2CO3溶液 |
持续产生较多气泡 |
|
| 2-4 |
向试管中加入2mL17.7%的X溶液 |
无明显现象 |
|
| 2-5 |
向试管中加入2mL1%的X溶液 |
无明显现象 |
【解释与结论】
①依据实验1-1、1-2的现象,可得出猜想1正确,补全实验1-1的现象。
②实验2-4、2-5中加入的X是。
③得出“Na2CO3溶液浓度越大,反应更剧烈”的结论,依据的实验是(填编号)。
④实验2的结论是。
⑤欲进一步检验反应产生的白色沉淀中是否含有碳酸盐,所需试剂是。