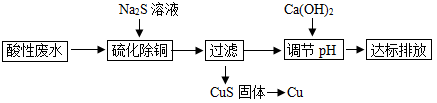
已知:硫化除铜时,溶液的pH会随着Na2S的加入量增多而逐渐增大。当溶液的pH<3.13时,发生的主要反应是 ,当溶液的pH>3.13时,发生的主要反应是
。

①从微观角度分析反应开始时Cu2+浓度逐渐下降的原因:。
②当Na2S的加入量超过0.8g·L-1后,溶液中剩余的Cu2+浓度几乎不再随Na2S的加入而改变,可能的原因是。
①炼制过程中,Cu元素的化合价发生的变化为。
②SO2会污染环境,其化学性质与CO2有相似之处,故可用(填化学式)与之反应生成CaSO3而将其除去。