①写出硼氢化钠与水反应的化学方程式:。
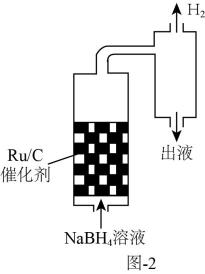
②已知粘度越大的液体,阻止微晶下沉的效果越好。相同温度下,将不同浓度的NaBH4溶液以相同的流速通过装有Ru/C催化剂的反应器(装置见图2)。质量分数为10%的NaBH4溶液通过反应器后,测得出液口溶液粘度为4.68mPa·s;质量分数为15%的NaBH4溶液通过反应器后,测得出液口溶液粘度为10.42mPa·s。不同质量分数的溶液反应50小时后,Ru/C催化剂的活性在15%的NaBH4溶液中大于10%的NaBH4溶液的原因是。

①若使用H218O代替H2O分解制氢,则获得的氧气可能是(填字母)。
a.O2 b.18O2 c.Ol8O
②补充完成TiO2材料光催化分解水制氢的过程描述:在紫外光的照射下,TiO2材料的VB端将电子转移至CB端,。