
图1

①图2可知,其他条件不变,随温度升高,CO2的平衡转化率先上升后下降,“先升高”的原因是;“后下降”的原因是由于设备腐蚀加剧等因素造成CO2的平衡转化率下降。
②下列说法正确的是。
A.图2两曲线中L1<L2
B.增大氨碳比有利于提高尿素产率,过量氨气能与水蒸气作用促进第二步反应正移
C.图3曲线M1>M2 , 增大水碳比有利于尿素生成
D.实际工业生产时,可选用初始条件为氨碳比L1和水碳比M1
③若已知M1>M0 , 请在图2中画出在初始L1和M1条件下,CO2的平衡转化率随温度变化曲线。
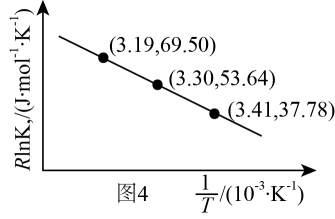
已知:RlnKp=-+C(C为常数)。根据图4计算该反应△H=kJ·mol-1。