1.
(2022高一上·十堰期中)
现有一不纯的小苏打样品(含杂质NaCl、Na2CO3·10H2O),为测定NaHCO3的质量分数,设计如图所示的实验装置(夹持仪器未画出)。
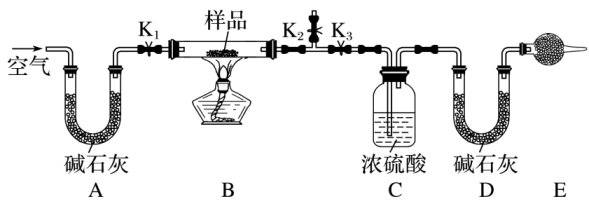
实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取一定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2 , 关闭K3 , 缓缓鼓入空气数分钟。
④关闭活塞K1、K2 , 打开K3 , 点燃酒精灯加热至不再产生气体。
⑤打开活塞K1 , 缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
[资料]
i.浓硫酸常用于吸收水蒸气。
ii.碱石灰是固体氢氧化钠和氧化钙的混合物。
iii.Na2CO3·10H2O Na2CO3+10H2O↑。
Na2CO3+10H2O↑。
回答下列问题:
-
(1)
仪器E的名称是,其中盛放的药品是;若无该装置,则会导致测得的NaHCO3的质量分数(填“偏大”“偏小”或“无影响”)。
-
-
-
-
(3)
装置B中除反应Na
2CO
3·10H
2O

Na
2CO
3+10H
2O↑外,还发生反应的化学方程式为
。
-
-
(4)
若实验中称取样品的质量为 50.0 g,反应后C、D装置增加的质量分别为12.6 g、8.8 g,则混合物中NaHCO3的质量分数为%(计算结果精确到0.1);若将等质量的该样品与足量稀硫酸混合,可得CO2的质量为g(计算结果精确到0.1)。
-

Na2CO3+10H2O↑。