选项 | 待提纯的物质 | 选用的试剂 | 操作的方法 |
A | 水 | 溶解、过滤、结晶 | |
B | 稀盐酸 | 溶解、过滤、洗涤、干燥 | |
C | 氢氧化钠溶液 | 过滤 | |
D | 氧气 | 点燃 |

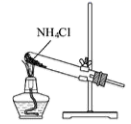 制取氨气
B .
制取氨气
B . 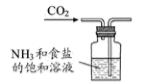 制取碳酸氢钠
C .
制取碳酸氢钠
C . 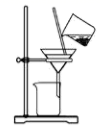 分离碳酸氢钠
D .
分离碳酸氢钠
D . 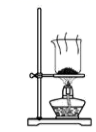 干燥碳酸氢钠
干燥碳酸氢钠
以上物质能导电的是。
Ⅰ 向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ 向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ 将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有 (用离子符号表示,下同);一定没有;可能含有,检验是否存在该离子的方法为。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为。
氯气(Cl2) | KMnO4 | PbO2 |
有刺激性气味,呈黄绿色,有毒气体 | 易溶于水,溶液呈紫红色,可用于杀菌消毒 | Pb的最高化合价为+4,其稳定化合价为+2,难溶于水,灰色固体 |
滴加适量H2O2 , 紫红色褪去,并有无色气泡产生;再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
①在配制酸性KMnO4溶液时,能否用盐酸?,原因是。
②KMnO4、H2O2、PbO2的氧化性由强到弱的顺序为。
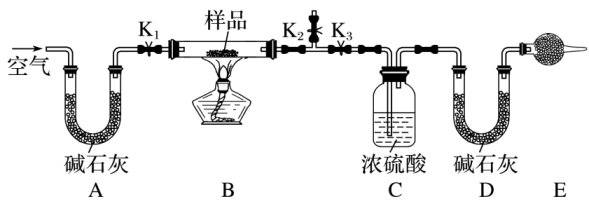
实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取一定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2 , 关闭K3 , 缓缓鼓入空气数分钟。
④关闭活塞K1、K2 , 打开K3 , 点燃酒精灯加热至不再产生气体。
⑤打开活塞K1 , 缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
[资料]
i.浓硫酸常用于吸收水蒸气。
ii.碱石灰是固体氢氧化钠和氧化钙的混合物。
iii.Na2CO3·10H2ONa2CO3+10H2O↑。
回答下列问题: