
①若向NaOH溶液中通入SO2制取NaHSO3溶液,则当溶液的pH为 时应停止通入。
②向NaOH溶液中通入SO2 , 所得溶液中一定存在的等式是 (用溶液中所含微粒的物质的量浓度表示)。
③NaHSO3溶液的酸碱性: 。
④若测得25℃时,某溶液中c(SO32-)/c(H2SO3)=10,则溶液的pH为。
① 如何判断滴定终点:。
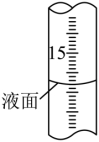
②滴定过程中,滴定管液面如图所示,此时滴定管的读数为 mL。
③计算久置Na2SO3固体中Na2SO3的质量分数为
④ 下列情况会造成样品中Na2SO3含量测定结果偏低的是 (填序号)。
A.滴定过程中用蒸馏水冲洗锥形瓶瓶壁
B.装Na2S2O3标准溶液的滴定管水洗后未润洗
C.开始滴定时,滴定管尖嘴部分未充满液体
D.滴定前仰视读数,滴定后俯视读数