【资料信息】
①Cu2O可与稀硫酸反应,化学方程式为:;
②Cu2O受热时可被H2还原为Cu;
③浓硫酸和碱石灰具有吸水性;
④无水硫酸铜固体遇水变蓝;
⑤锌与浓硫酸反应产生有刺激性气味的气体,该气体是形成酸雨的主要气体。
【还原实验】
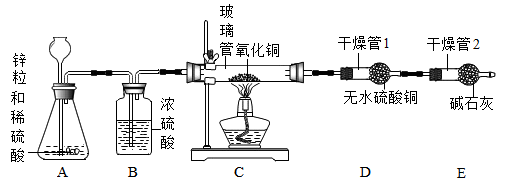
连接上图实验装置,检查装置气密性,在A装置中加入稀硫酸,点燃C处酒精灯加热,观察到黑色固体变红,无水硫酸铜变蓝,当黑色固体完全变红后,移去酒精灯,待C装置固体冷却后,停止通入氢气。
猜想一:固体产物全是Cu;
猜想二:固体产物。
猜想三:固体产物中既有Cu也有Cu2O。
探究过程 | 现象 | 结论 |
取少量红色固体于试管中,加入过量稀硫酸 | 猜想一不成立 | |
另取ag红色固体于试管中,在氢气流中加热至固体质量不再变化,称得固体质量为 | 砖红色固体变为红色 | 猜想成立 |
根据探究结果,写出H2还原CuO的化学反应方程式。
在制取氢气时,该学习小组成员不小心把浓硫酸当成稀硫酸使用,导致实验进行到后阶段才能观察到黑色的氧化铜逐渐变为红色,请解释原因,写出锌和浓硫酸反应的化学方程式。