 往试管送入粉末
B .
往试管送入粉末
B . 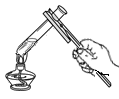 加热液体药品
C .
加热液体药品
C .  熄灭酒精灯
D .
熄灭酒精灯
D .  读取液体体积
读取液体体积
选项 | 劳动项目 | 化学知识 |
A | 用燃气灶炒菜 | 燃气燃烧放热 |
B | 使用煤炉时,用扇子往炉中扇风 | 空气流通,提供充足的氧气 |
C | 炒菜时油锅着火,用锅盖盖灭 | 降低油的着火点 |
D | 用淘米水洗菜 | 爱护水资源,节约用水 |
选项 | 实验目的 | 实验操作 |
A | 验证质量守恒定律 | 碳酸钠和稀盐酸在敞口容器中反应 |
B | 除去氧化铜中混有的碳粉 | 在氧气流中充分加热混合物 |
C | 除去氧化钙中混有的少量碳酸钙 | 加水溶解、过滤、洗涤、干燥 |
D | 探究锌、铁、铜的金属活动性顺序 | 将铜丝、铁丝分别插入硫酸锌溶液中 |
 加热两份等质量的氯酸钾制取氧气
B .
加热两份等质量的氯酸钾制取氧气
B . 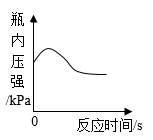 用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
C .
用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
C . 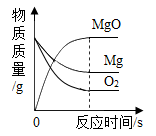 等质量的镁和氧气充分反应
D .
等质量的镁和氧气充分反应
D . 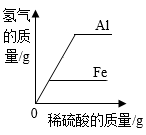 向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸
向等质量的铝粉和铁粉中分别加入溶质质量分数相等的稀硫酸
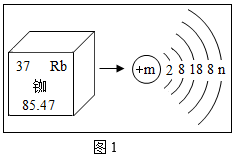
A.一氧化碳 B.钙 C.氧气 D.臭氧 E.氖气 F.不锈钢 G.酒精 H.四氧化三铁
①原子种类 ②分子种类 ③分子数目 ④元素种类


物质 | CoO | Co3O4 | Co(OH)2 | CoCl2 | CoSO4 |
物理性质 | 灰色固体 难溶于水 | 黑色固体 难溶于水 | 蓝绿色固体 难溶于水 | 蓝色固体 易溶于水 成粉红色溶液 | 玫瑰红色固体 易溶于水 成粉红色溶液 |
请你设计实验证明钴的金属活动性比铜的强。
实验方案 | 实验现象 |

【资料信息】
①Cu2O可与稀硫酸反应,化学方程式为:;
②Cu2O受热时可被H2还原为Cu;
③浓硫酸和碱石灰具有吸水性;
④无水硫酸铜固体遇水变蓝;
⑤锌与浓硫酸反应产生有刺激性气味的气体,该气体是形成酸雨的主要气体。
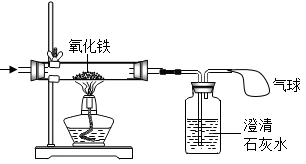
【还原实验】
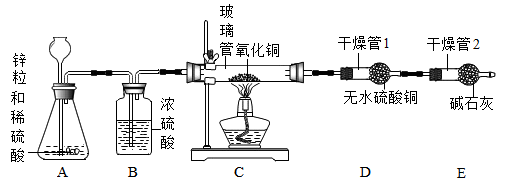
连接上图实验装置,检查装置气密性,在A装置中加入稀硫酸,点燃C处酒精灯加热,观察到黑色固体变红,无水硫酸铜变蓝,当黑色固体完全变红后,移去酒精灯,待C装置固体冷却后,停止通入氢气。
猜想一:固体产物全是Cu;
猜想二:固体产物。
猜想三:固体产物中既有Cu也有Cu2O。
探究过程 | 现象 | 结论 |
取少量红色固体于试管中,加入过量稀硫酸 | 猜想一不成立 | |
另取ag红色固体于试管中,在氢气流中加热至固体质量不再变化,称得固体质量为 | 砖红色固体变为红色 | 猜想成立 |
根据探究结果,写出H2还原CuO的化学反应方程式。
在制取氢气时,该学习小组成员不小心把浓硫酸当成稀硫酸使用,导致实验进行到后阶段才能观察到黑色的氧化铜逐渐变为红色,请解释原因,写出锌和浓硫酸反应的化学方程式。
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
瓶中物质总质量(g) | 42.4 | m | 82.0 | 101.8 | 121.8 |
(假设铁合金样品中只含有铁、碳两种元素)
请回答下列问题: