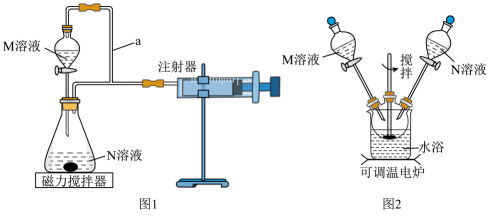
实验Ⅰ.在光亮处将M溶液一次性放入锥形瓶中并不断搅拌,然后关闭活塞。
实验Ⅱ.用黑纸袋包住锥形瓶后再将M溶液一次性放入锥形瓶中并不断搅拌,然后关闭活塞。
两次实验所用M溶液与N溶液相同。
①检查图1装置气密性的方法为。
②盛装M溶液的仪器名称为,a的作用是。
③该实验探究的是对化学反应速率的影响。
④在反应停止前,相同时间内注射器中所得CO2的体积较多的是(填“实验Ⅰ”或“实验Ⅱ”)。
实验时将M溶液和N溶液同时加入三颈烧瓶中,并不断搅拌,M、N的成分以及水浴温度如下表:
序号 | M溶液 | N溶液 | 水浴温度 |
A | 含0.01mol碘的四氯化碳溶液20mL | 20mL0.4 mol·L-1的K2C2O4溶液 | 40℃ |
B | 含0.01mol碘的四氯化碳溶液20mL | 20mL0.8 mol·L-1 | 40℃ |
C | 含0.01mol碘的四氯化碳溶液20mL | 20mL0.8 mol·L-1的K2C2O4溶液 | 50℃ |
①该实验探究的是对化学反应速率的影响。
②该组同学始终没有观察到实验A的溶液褪色,其原因是。