I.制备碳酸亚铁:装置如图所示。
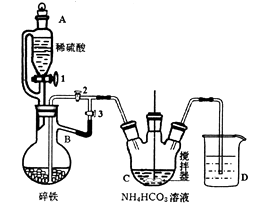
向纯净的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。
该反应方程式为。为防止乳酸亚铁变质,在上述体系中还应加入。反应结束后,将所得溶液隔绝空气低温蒸发、冷却结晶、过滤、洗涤、干燥得乳酸亚铁晶体。该晶体存放时应注意。
两位同学分别用不同方案进行测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度,所得纯度总是大于100%,其原因可能是。
②乙同学经查阅文献后改用(NH4)4Ce(SO4)4滴定法测定样品中Fe2+的含量计算样品纯度(反应中Ce4+还原为Ce3+),称取6.00g样品配制成250.00mL溶液,取25.00mL用0.10mol·L-1(NH4)4Ce(SO4)4标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为(以质量分数表示)。