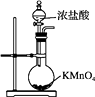
 B . 除去Cl2中的HCl
B . 除去Cl2中的HCl  C . 氯气的尾气处理
C . 氯气的尾气处理 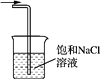 D . 测氯水的pH
D . 测氯水的pH 
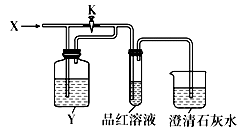
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
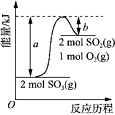

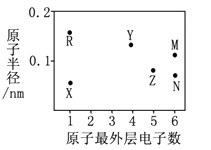
某化工生产的核心环节的反应为:2MN2(g) + N2(g) ⇌ 2 MN3(g) + Q(Q>0)
0.1mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线如图甲所示:
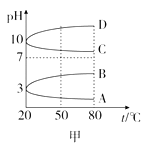
25℃时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图乙所示。

i. 含有苯环 ii. 含有醛基:
取少量ClCH2COOH置于试管中,,加热,,滴加硝酸银溶液,观察是否产生白色沉淀。
 的合成路线(其它试剂任选)。
的合成路线(其它试剂任选)。
学生甲利用下图装置进行实验:加热A中试管内装有的潮湿漂白粉样品时,观察到B中有大量气泡产生。
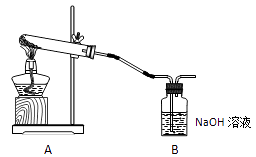
学生乙设计实验测定某干燥漂白粉样品中次氯酸钙的百分含量。实验步骤如下:
①称量坩埚的质量,为W1g。
②坩埚中加入样品后再称,质量为W2g。
③重复进行加热、冷却、称量,直到恒重,质量为W3g。