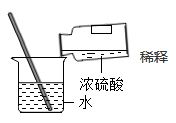
 稀释
B .
稀释
B . 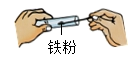 取药
C .
取药
C .  称量
D .
称量
D . 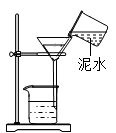 过滤
过滤
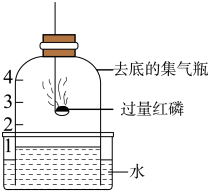
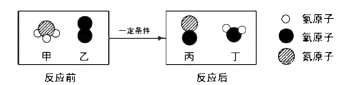
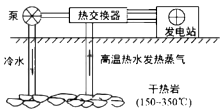
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。
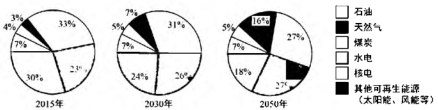
由上图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用是热门研究方向之一。例如,通过光催化可将H2O、CO2转化为H2、CO、CH4、CH3OH(甲醇)等太阳能燃料,示意图右图。
随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电。

在新能源的开发和利用中,化学起着不可替代的作用。
依据文章内容回答下列问题。
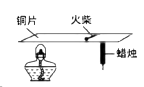
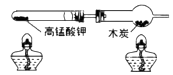
【查阅资料】①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+ H2SO4 = CuSO4 + H2O + Cu
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
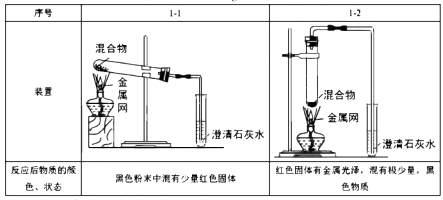
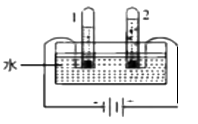
实验2:取一定量的混合物,用1—2装置进行实验。
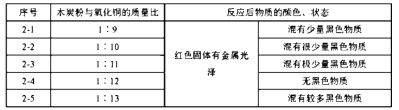
【解释与结论】
实验2没有进行质量比为1:14的实验,理由是。