

用品 | 小苏打 | 管道通 |
有效成分 | NaHCO3 | NaOH |

你吃过木糖醇口香糖吗?
木糖醇为白色固体,极易溶于水,溶解时吸收大量热,甜度与蔗糖相当。
木糖醇广泛存在于各种水果、蔬菜、谷类中,但含量很低。商品木糖醇是将玉米芯、甘蔗渣等农作物进行深加工制得的。我国木糖醇生产工艺路线如下:原料→水解→中和→……. →加氢、结晶→包装。其中原料水解时用硫酸做催化剂,再用碳酸钙将硫酸除去。
龋病是人类常见的一种口腔疾病,其发生过程中不可缺少的微生态环境是牙菌斑。目前普遍认为,牙菌斑中的细菌在代谢食物中糖类的过程中产生酸性物质,酸性物质可导致牙釉质溶解,进而形成龋病。牙菌斑pH 变化可反映牙菌斑内产生酸性物质的情况。
木糖醇不致龋且有防龋齿的作用。第三军医大学韩旭对木糖醇防龋过程进行了研究,部分内容如下。
研究1:用10%的蔗糖、葡萄糖、木糖醇溶液漱口,牙菌斑pH的变化

研究2:用蔗糖溶液涑口后咀嚼口香糖,牙菌斑pH的变化

研究表明,饭后咀嚼木糖醇口香糖可以起到防龋的作用,可以明显降低患龋率。
依据文章内容,回答下列问题。

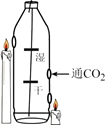


【提出问题】如何能观察到反应的变化过程?
【查阅资料】
NaOH、Na2CO3在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 |
NaOH | 42 | 51 | 109 | 119 |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaOH、Na2CO3在乙醇中的溶解度
温度/℃ | NaOH | Na2CO3 |
18.5~25 | 17.3 | 不溶 |
【进行实验】注:乙醇在实验中只作为溶剂,不参与化学反应。
实验 | 实验装置 | 实验操作 | 实验现象 |
1 |
| 打开止水夹,通入 CO2 , 气球明显鼓起后关闭止水夹 | 一段时间后,气球明显变瘪 |
2 |
| 室温下,向10mL澄清饱和的NaOH溶液中通入适量CO2 | 试管内壁出现白色固体 |
3 |
| ① 室温下,向10mL饱和的NaOH乙醇溶液中缓慢通入适量CO2 | 甲中出现白色沉淀,乙中无明显现象 |
② 滴入稀盐酸 | 甲中有气泡生成,乙中澄清石灰水变浑浊 |
【解释与结论】
实验1是从(填“反应物消耗”或“新物质生成”)角度证明化学反应发生。