 氧气可以使带火星的木条复燃
B .
氧气可以使带火星的木条复燃
B . 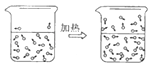 水受热蒸发
C .
水受热蒸发
C .  液体混合产生气体
D .
液体混合产生气体
D .  葡萄酿成美酒
葡萄酿成美酒
 B .
B .  C .
C .  D .
D . 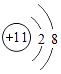
选项 | A | B | C | D |
实验设计 |
|
|
|
|
实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明水是由氢元素和氧元素组成的 | 只能证明二氧化碳的密度比空气大 | 证明铁生锈是水和氧气共同作用的结果 |
选项 | 物质 | 选用试剂 | 操作 |
A | CO2(CO) | O2 | 点燃 |
B | N2(O2) | C | 点燃 |
C | FeSO4溶液(CuSO4) | Fe | 加入过量的试剂,过滤 |
D | CaO(CaCO3) | H2O | 加水,搅拌 |
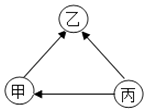
甲 | 乙 | 丙 | 丁 | |
A | Fe2O3 | CO | O2 | C |
B | HCl | Cu | AgNO3 | Zn |
C | CaCO3 | HCl | Cu | O2 |
D | H2 | O2 | Fe | HCl |

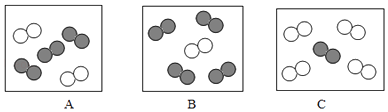
同温同压下,气体的体积比等于分子数目比.若空气中其它成分忽略不计,图中可表示空气微观模型的是(填标号).
Ⅰ、已知:常温下,氮气沸点﹣196℃,氧气沸点﹣183℃.因此工业上分离液态空气制取氧气时,首先从液态空气中蒸发出来.
Ⅱ、空气中氧气含量的测定
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).
该实验中选择使用汞的优点有.
A.能将密闭装置内空气中的氧气几乎耗尽
B.在汞槽中起到液封的作用
C.生成的化合物加热分解又能得到汞和氧气
D.实验过程中没有污染
某兴趣小组用图2测定空气中氧气的含量.在空气中点燃红磷的实验过程,固体变化如图3所示.

①从燃烧条件分析,固体质量在t 1前没有发生变化的原因为.
②该反应的化学方程式为.
③参加反应的氧气质量为 g.

①Ⅰ中参加反应的单质甲为.
②Ⅱ中反应的化学方程式为.
③物质所含元素化合价发生变化的反应称为氧化还原反应.反应Ⅲ(填“属于”或“不属于”)氧化还原反应.

【提出问题】生成的气体中是否含有一氧化碳?
兴趣小组同学利用图2所示的装置进行实验,对生成的气体成分进行探究.
【实验与讨论】
①打开K,缓缓通入干燥的氮气一段时间.
②关闭K,加热至一定温度使玻璃管中的炉甘石、赤铜和木炭粉反应,用气囊收集气体样品.
③欲除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列图3装置中最为合理的是.

【实验求证】将除尽二氧化碳后的气体样品干燥,仍然用图2所示的装置进行实验,A中的固体应选用,B中溶液为澄清石灰水,若A中黑色固体出现了红色,B中澄清石灰水,其化学方程式为,可说明气体样品中含有一氧化碳.
【实验反思】上述实验中,若生成的气体中含有一氧化碳,则反应时消耗碳、氧元素的质量比(填“大于”、“等于”或“小于”)3:8.
①甲同学说是铜、锌合金.乙同学说可能是金.
其他的同学否定了乙同学的猜测.其理由是.
②为测定该黄铜(铜、锌合金)中铜的质量分数,某兴趣小组取20g黄铜样品放入盛有200g稀硫酸的烧杯中,恰好完全反应,测得烧杯中剩余物质的总质量为219.8g,则:该黄铜样品中铜的质量分数为.(计算结果保留0.1%)

③有的兴趣小组用图4装置测定黄铜中铜的质量分数.下列关于该实验的说法正确的是
A.分液漏斗与试管间的橡胶管仅有使液体顺利下滴的作用
B.若实验中稀硫酸不足,可以拔下分液漏斗上方的橡皮塞添加
C.该测定还需要的数据是样品质量和此温度、压强下氢气的密度
D.实验结束时,需冷却至室温并将量气管缓缓下移至两侧液面相平再读数
①某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图5所示,则:
a.溶液甲中一定含有Al(NO3)3和Zn(NO3)2
b.固体乙中一定含有Ag,可能含有Cu和Zn
c.若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2
d.向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2
上述四种说法正确的个数为
A.1个 B.2个 C.3个 D.4个
②利用废旧电池铜帽(含Cu、Zn)提取Cu,并得到ZnSO4溶液,主要流程如图6,(已知:①反应条件已略去;②2Cu+2H2SO4+O2 2CuSO4+2H2O).

a.溶液A和固体C都含有两种元素,过程Ⅱ、Ⅲ中的分离操作是.
b.请写出步骤Ⅲ中发生反应的化学方程式:.