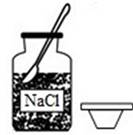
 B . 称固体
B . 称固体 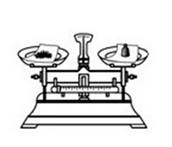 C . 量取水
C . 量取水 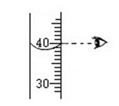 D . 写标签
D . 写标签 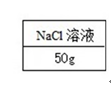
 B . 比较黄铜与纯铜的硬度
B . 比较黄铜与纯铜的硬度  C . 探究二氧化碳能与水反应
C . 探究二氧化碳能与水反应  D . 比较呼出的气体与空气中的氧气含量
D . 比较呼出的气体与空气中的氧气含量 


|
元素名称 |
钠 |
镁 |
铝 |
硅 |
磷 |
硫 |
氯 |
|
核电荷数 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
|
常见化合价 |
+1 |
+2 |
+3 |
-4、+4 |
-3、+5 |
-2、+4、 +6 |
-1、+7 |
|
最外层的电子数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
两个磷原子,铝离子,硫元素的最高正价氧化物。
 X的数值为。
X的数值为。 根据n的数值,可推断在化学变化过程中,氯原子容易(填“失去”或“得到”)电子。
![]()
粗盐的初步提纯过程是:溶解→过滤→蒸发,这三步操作中都用到的一种玻璃仪器是。

①将步骤Ⅱ反应的化学方程式补充完整:+H2SO4 ![]() CuSO4+H2O
CuSO4+H2O
②古代“湿法冶金”的原理与图中步骤(填“Ⅰ”、“Ⅱ”或“Ⅲ”)的反应原理相同。
③利用化学方法从“不溶物A”中提纯铜单质:(用化学方程式表示)。

|
实验编号 |
盐酸的质量分数 |
镁的形态 |
溶液初始温度/℃ |
|
① |
3% |
粉末 |
30 |
|
② |
3% |
条状 |
20 |
|
③ |
6% |
粉末 |
20 |
|
④ |
6% |
条状 |
20 |
图1  图2
图2 
图3 