 B .
B .  C .
C .  D .
D . 
| 植物 | 胡萝卜 | 土豆 | 西红柿 | 南瓜 |
| 适宜的pH范围 | 5.0~6.0 | 4.8~5.4 | 6.0-7.0 | 6.0-8.0 |

①过氧化钠属于氧化物 ②该反应属于置换反应 ③反应前后部分氧元素化合价发生了变化 ④实验室可利用这一原理制取纯净的氧气。

①取少量该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。向该溶液中加入适量的硝酸银溶液,有白色沉淀产生,再加入足量的稀硝酸,充分反应后,部分白色沉淀消失。
②另取13.8g该粉末于烧杯中,加水使其完全溶解,再加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,过滤后得到19.7g白色沉淀和滤液a。
下列说法正确的( )

A 只有固体 B 只有液体 C 只有气体 D 气体、液体、固体都可以
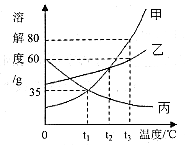
①将一瓶接近饱和的丙溶液变成饱和溶液,除通过增加溶质、蒸发溶剂使其达到饱和外,还可采取的方法。
②将t3℃时等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的质量由大到的顺序为。
③t3℃时,取甲、乙两物质配制溶液。
| 序号 | a | b | c | d | e |
| 固体种类 | 甲 | 甲 | 甲 | 乙 | 乙 |
| 甲固体的质量/g | 30 | 60 | 90 | 30 | 60 |
| 水的质量/g | 100 | 100 | 100 | 100 | 100 |
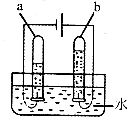
他让水蒸气通过一根高温烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为;
实验I:硝酸银溶液和铁粉混合
实验II:硝酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验I和II的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多。充分反应后过滤,向滤渣中滴加盐酸,没有气泡产生。则滤液中一定含有的溶质为(填化学式,下同),可能含有的溶质为。
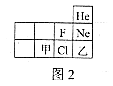
①C+D=A+2F ②2E+D=B+2F ③A+2E=C↓+B
根据上述信息回答问题:
反应①;
反应③。


①同学们在实验室用浓硫酸配制稀硫酸,除用到胶头滴管、量筒、烧杯外,还需要用到的仪器有。
②实验室用98%的浓硫酸(密度1.84g/mL)配制24.5%的硫酸溶液1200g,需要98%浓硫酸的体积为mL(计算结果保留至0.1)。