 取用
B .
取用
B .  称取
C .
称取
C . 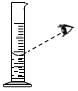 量取
D .
量取
D .  溶解
溶解
 一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
B .
一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉
B .  等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
C .
等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
C .  等质量的铁粉和锌粉分别与足量溶质质量分数相同的稀硫酸反应
D .
等质量的铁粉和锌粉分别与足量溶质质量分数相同的稀硫酸反应
D .  高温条件下一氧化碳还原氧化铁
高温条件下一氧化碳还原氧化铁
图一  图二
图二 
图三 
①写出仪器a的名称。
②实验室常用图一装置来制取氢气,反应的化学方程式为,该装置的优点是。
③若用稀盐酸制取氢气,会含有少量杂质,用图二装置可得到干燥、纯净的氢气,导管气流方向接接顺序正确的是(填字母)。

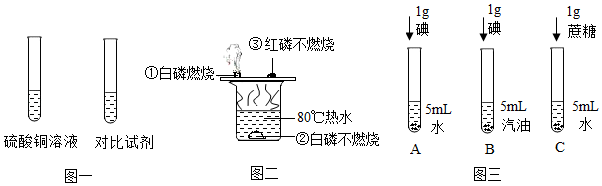
②同学们又补充了试管C所示实验,他们想探究的影响物资溶解性的因素是。

请回答下列问题:

由实验现象和曲线变化情况分析可知,盐酸和氢氧化钠溶液发生了反应并(填“吸收”或“放出”)热量。

由如图可知,该反应的微观实质是。
(交流讨论)同学们讨论后认为,如果盐酸和氢氧化钠减少(或消失),或者有新物质生成,都能证明反应已经发生。
|
步骤 |
现象 |
结论 |
|
实验1:取烧杯中的溶液少许于试管中,加入硫酸铜溶液 |
|
证明没有NaOH |
|
实验2;另取烧杆中的溶液少许于试管中,加入硝酸银溶液 |
出现白色沉淀 |
证明含有HCl |
|
实验3:再取烧杯中的溶液少许于蒸发皿中,加热蒸干 |
有产生 |
证明有NaCl生成 |
(得出结论)氢氧化钠溶液和盐酸发生了中和反应。
Ⅰ.有同学认为,仅通过实验2出“溶液中含有HCl”证据不足,理由是。
Ⅱ.运用中和反应,可以解决生产,生活中的实际同题。如工厂用氨水(NH3•H2O)处理废水中的硫酸,能得到一种氮肥一硫酸铵,写出该反应的化学方程式。
Ⅲ.多角度认识少学反应是学习化学的重变方法。